Coenzymes et vitamines

1
Coenzymes et vitamines
PCEM1 année 2009-2010
Coenzymes et vitamines
Introduction et Généralités
Vitamines
Coenzymes
Coenzymes d’oxydoréduction
Coenzymes redox hydrosolubles vitaminiques
Coenzymes redox non vitaminiques
Coenzymes redox liposolubles vitaminiques
Coenzymes de transfert de groupements
Coenzymes de transfert hydrosolubles du groupe B
Coenzymes de transfert hydrosolubles non vitaminiques

2
Généralités : Vitamines
I- Généralités sur les vitamines
Historiquement « vitamine » est un terme signifiant : “ amine bénéfique à la vie ”
cependant les composés appelés vitamines ne comportent pas tous une fonction
« amine ».
De nature organique
En général non synthétisées par l’organisme :
- notion variable selon les espèces considérées : il peut exister une voie de
biosynthèse endogène
Chez l’Homme
soit apport alimentaire obligatoire
soit synthèse par les bactéries intestinales
Utiles en petites quantités pour assurer leurs fonctions biochimiques
Concentration faible dans le sang
Apport exogène
Végétal
Autres espèces
Généralités : Vitamines
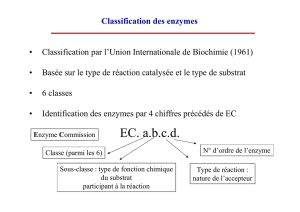
II- Classification
Les vitamines hydrosolubles
vit C (Ac Ascorbique) + vit du groupe B
groupe B : B1, B2, B3 ou PP, B5, B6, B8 ou H, B9, B12
Hydrosoluble = absence de stockage dans l’organisme
nécessité d’un apport régulier
pas de toxicité en cas de surdosage (élimination urinaire)
Les vitamines liposolubles
A, D, E, K : apolaires, solubles dans les graisses
donc stockées dans l’organisme et potentiellement toxiques
en excès, elles entraînent des hypervitaminoses
NB : Vit A et D ne sont pas impliquées dans la structure de Coenzymes

3
Coenzymes et vitamines
Introduction et Généralités
Vitamines
Coenzymes
Coenzymes d’oxydoréduction
Coenzymes redox hydrosolubles vitaminiques
Coenzymes redox hydrosolubles non vitaminiques
Coenzymes redox liposolubles vitaminiques
Coenzymes de transfert de groupements
Coenzymes de transfert hydrosolubles du groupe B
Coenzymes de transfert hydrosolubles non vitaminiques
Généralités : Coenzymes
I- définition cofacteur/coenzyme
Terme global : Cofacteur
de nature non organique
Plus de 25% de toutes les enzymes nécessitent la présence d’un
cofacteur métallique :
cations divalents Mg++, Ca++, Mn++, Fe++, Zn++, Cu++
Soit nécessaire à l’action de l’enzyme mais sans liaison étroite
Soit fortement lié à la protéine et purifié avec elle
de nature organique non protéique
Coenzymes : de petite taille, de structure souvent cyclique.
Parmi lesquels on distingue
les groupements prosthétiques, liés par covalence à l’apoenzyme
les co-substrats ou coenzymes libres car faiblement liés à la protéine.

4
E1
Généralités : Coenzymes
II- Propriétés des coenzymes
Lié plus ou moins fortement à l’apoenzyme, le coenzyme (CoE) fait partie
intégrante du mécanisme catalytique
Groupement prosthétique
- fortement lié au site actif de l’enzyme par des liaisons covalentes (comme un
pont peptidique)
- régénéré à la fin de la réaction
-
régénéré à la fin de deux réactions couplées au sein d’un même complexe
enzymatique
Co-substrat ou CoE libre
- fixé réversiblement au site actif par des liaisons faibles
- régénéré au cours d’une réaction catalysée par une deuxième enzyme dans la
même voie métabolique ou dans une autre voie métabolique
CoE
E2
Généralités : Coenzymes
III- Fonctions des coenzymes
transferts de groupements autres que H+
transfert d’e- et de protons au cours des réactions d’oxydo-réduction
Les enzymes nécessitant des coenzymes catalysent des réactions :
d’oxydo-réduction : oxydo-reductases EC1
de transfert de groupement : transférases EC2 toujours CoE
de formation de liaisons covalentes : ligases EC6
d’isomérisation : isomérases EC5 CoE facultatif

5
Deux parties dans la molécule
éléments de liaison à l'enzyme
(faible ou covalent)
partie réactive
Généralités : Coenzymes
GROUPEMENTS
IMPLIQUES
DANS LA
LIAISON
A L'ENZYME
PARTIE
REACTIVE
IMPLIQUEE
DANS LA
CATALYSE
Molécules organiques
Coenzymes
Gènes
Généralités : Coenzymes
III Relation entre Vitamines et coenzymes
Les mêmes composés sont des CoE chez tous les êtres vivants mais leur nature vitaminique
varie selon les espèces (selon qu’elles peuvent en produire de façon autonome ou pas)
Les co-enzymes sont des composés organiques
Biosynthèse grâce à
des enzymes
dont la production dépend de voies de biosynthèse comprenant une série de réactions
enzymatiques
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
1
/
22
100%