dossier greffe renale - Rein

DOSSIER GREFFE RENALE
mars -septembre 2012 - Reins-Échos n°12
///
25
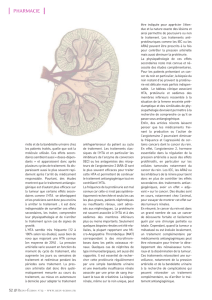
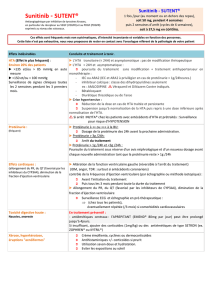
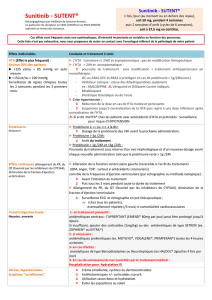
breux traitements antiangiogéniques
sont commercialisés ou font l’objet
de protocoles de recherche. Certains
s’administrent par voie intraveineuse
comme l’AVASTIN® (Bevacizumab)
toutes les semaines et d’autres par
voie orale en continu ou en cures
comme le SUTENT® (Sunitinib) ou le
NEXAVAR® (Sorafenib). Dans le can-
cer du rein, le plus utilisé est actuel-
lement le Sunitinib mais de nouvelles
molécules sont en cours d’étude. Le
plus souvent, ce traitement est uti-
lisé après la chirurgie de la tumeur
primitive, pour traiter les métastases
(traitement adjuvant). Cependant,
dans certains cas, il peut être prescrit
avant la chirurgie pour faire diminuer
le volume tumoral (traitement néo-
adjuvant), ou même en l’absence de
chirurgie si la tumeur n’est pas opé-
rable.
Cependant, le VEGF est aussi indis-
pensable aux vaisseaux normaux et
tous ces traitements peuvent donc
entraîner des effets secondaires. A
coté des effets digestifs classiques
avec les chimiothérapies anticancé-
reuses (diarrhées, vomissements,
fatigue) on peut voir se développer
des effets secondaires rénaux comme
l’hypertension artérielle (HTA) par-
fois sévère, une protéinurie (protéines
dans les urines), ou une insuffisance
rénale par différents mécanismes.
La fréquence de ces effets secon-
daires n’est pas connue avec préci-
sion mais semble suffisamment éle-
vée pour justifier un contrôle régulier
de la pression artérielle et de la ban-
delette urinaire chez les patients trai-
tés, quelle que soit la molécule utili-
sée. Ces effets secondaires semblent
aussi « doses-dépendants » et appa-
raissent donc après plusieurs cycles
de traitement. Ils disparaissent aussi
le plus souvent rapidement après
l’arrêt du médicament responsable.
Pourtant, des études montrent que le
traitement antiangiogénique est d’au-
tant plus efficace sur la tumeur que
certains effets secondaires comme
l’HTA se développent et les praticiens
sont donc peu enclins à arrêter le trai-
tement ; il est donc indispensable de
surveiller ces effets secondaires, les
traiter, comprendre leur physiopa-
thologie et de n’arrêter le traitement
qu’en cas de signes de gravité.
L’HTA semble très fréquente (12 à
100% selon les études), aussi bien de
novo que majorant une HTA connue
(en moyenne de 20 %). La pression
artérielle varie souvent en fonction du
moment du cycle de traitement, elle
augmente les jours ou semaines de
traitement et rediminue pendant les
périodes sans traitement. La pres-
sion artérielle doit donc être systéma-
tiquement mesurée au cours du trai-
tement, au mieux en automesure à
domicile pour adapter le traitement
antihypertenseur du patient au cycle
de traitement. Les traitements clas-
siques de l’HTA et en particulier les
inhibiteurs de l’enzyme de conversion
(IEC) ou les antagonistes des récep-
teurs de l’angiotensine 2 (ARA-2) sont
le plus souvent efficaces pour traiter
cette HTA et permettent de continuer
le traitement antiangiogénique tout en
contrôlant l’HTA.
La fréquence de la protéinurie est mal
connue car celle-ci n’est pas systé-
matiquement recherchée et seuls les
cas les plus graves, patients néph-
rotiques ou insuffisants rénaux, sont
adressés aux néphrologues. La pro-
téinurie est souvent associée à l’HTA
et à des oedèmes des membres infé-
rieurs plus ou moins importants. Seu-
lement quelques biopsies rénales
ont été réalisées, la plupart rappor-
tant une Micro-Angiopathie Throm-
botique (MAT) correspondant à des
microthromboses dans les petits
vaisseaux rénaux. Quelques cas de
néphrites de type immunoallergiques,
ont aussi été rapportés. Il est essen-
tiel de rechercher cette protéinurie
régulièrement par une simple bande-
lette urinaire et une éventuelle insuf-
fisance rénale associée par une prise
de sang évaluant le taux de créatinine.
La biopsie rénale, même sur le rein
unique, peut être indiquée pour appré-
cier l’étendue et la nature exacte des
lésions et ainsi permettre de pour-
suivre ou non le traitement. Les trai-
tements antiprotéinuriques comme
les IEC ou les ARA2 peuvent être pres-
crits à la fois pour contrôler la pres-
sion artérielle mais aussi diminuer la
protéinurie.
La physiopathologie de ces effets
secondaires reste mal connue et
nécessite des études complémen-
taires. Pour les patients présentant un
cancer du rein en particulier, la biopsie
du rein restant d’où provient la protéi-
nurie est délicate mais parfois indis-
pensable. Le tableau clinique asso-
ciant HTA, protéinurie et oedèmes des
membres inférieurs ressemble à la
situation de la femme enceinte préé-
clamptique et des similitudes de phy-
siopathologie devraient permettre à la
recherche de comprendre ce qu’il se
passe sous antiangiogénique.
Enfin, des articles récents laissent
penser que les médicaments freinant
la production ou l’action de l’angio-
tensine 2 pourraient diminuer la fré-
quence et l’agressivité de certains can-
cers dont le cancer du rein. En effet,
l’angiotensine 2, hormone essentielle
dans la régulation de la pression arté-
rielle a aussi des effets prolifératifs,
en particulier sur les cellules tumo-
rales notamment du cancer du rein.
Les IEC, les ARA2 ou les inhibiteurs de
la rénine pourraient donc en plus de
contrôler les effets secondaires des
traitements antiangiogéniques, avoir
un effet « adjuvant » sur le cancer.
Des études sont en cours, notamment
chez l’animal, pour essayer de mon-
trer cet effet sur des tumeurs rénales.
En résumé, le cancer du rein est dans
un grand nombre de cas un cancer
de découverte fortuite et facilement
guéri par une chirurgie partielle ou
totale. Cependant, quand la tumeur a
métastasé ou est évoluée localement,
un traitement complémentaire par
médicaments antiangiogéniques peut
être nécessaire pour freiner le déve-
loppement des néovaisseaux tumo-
raux et la dissémination de la tumeur.
Ces traitements nécessitent une sur-
veillance, notamment de la pres-
sion artérielle et de la bandelette uri-
naire à la recherche de complications
qui peuvent nécessiter un traitement
complémentaire, ou d’arrêter le trai-
tement antiangiogénique. \\\
© A. Franski
1
/
1
100%