Développement du cortex cérébral : apports

Épilepsie et anomalies du développement du cortex cérébral
Épilepsie et anomalies du développement du cortex cérébral
Développement
du cortex cérébral :
apports récents des études
chez la souris et les primates
Nicolas Narboux-Nême, Patricia Gaspar
Inserm, U839, Paris, France et Université Pierre et Marie Curie, Paris, France
Institut du Fer à Moulin, 17 rue du Fer à Moulin, 75005 Paris
Résumé. La mise en place du cortex cérébral est une opération complexe qui met en jeu la production d’une
variété remarquable de neurones excitateurs et inhibiteurs. Ces neurones sont assemblés en circuits fonctionnels qui
s’organisent en couches et en aires. Le cortex a une expansion maximale chez l’homme, mais les grands principes de
son organisation et de son développement sont conservés chez tous les mammifères. Ainsi les approches génétiques
chez la souris, ont permis des avancées majeures de nos connaissances du développement cortical. On sait à présent
qu’il existe différentes sources de neurones corticaux, venant rejoindre des cellules précurseurs qui leur servent de
guide. Les gènes qui contrôlent la spécification, et la migration des neurones ont commencé à être identifiés, ainsi
que les mécanismes permettant l’établissement des connexions nerveuses. Les explorations conduites chez les
primates ont permis, de confirmer les observations faites chez le rongeur et dans certains cas d’identifier des
différences. Ainsi les neurones glutamatergiques et gabaergiques ont des origines différentes, chez les rongeurs,
alors que chez les primates, les interneurones proviennent majoritairement de la zone ventriculaire corticale, tout
comme les neurones glutamatergiques. Des différences de régulations de la prolifération de différents précurseurs
pourraient expliquer l’expansion du cortex des primates, en particulier des couches superficielles. Ces études
apportent un nouvel éclairage sur les pathologies du développement cortical qui vont des défauts précoces de la
corticogenèse jusqu’à des altérations subtiles du raffinement des connexions axonales.
Mots clés :cortex cérébral, développement, corticogenèse, lamination, raffinement axonal
Abstract. Development of the cerebral cortex : recent findings from studies in mouse and primate
The development of the cerebral cortex is a protracted process implying the generation of many different neuronal
cell types. These neurons organize in layers and set functional networks and areas whose function range from basic
perception to abstract thought. Although cerebral cortex has a very large expansion in human, its development is
quite similar in mammals, from rodent to primates. Studies conducted in mice, using genetic approaches, allowed
great advances in our understanding of cerebral cortical development during the last decade. Several sources for the
cortical neurons were discovered, as well as different classes of pioneer cortical neurons. Tremendous progress has
been made over these last years in identifying genes that specify the identity of cortical neurons, their migration
pattern, as well as more complex features of their organization such as arealization, and axon network formation.
Tirés à part :
N. Narboux-Nême
220
E
´pilepsies, vol. 20, n° 4, octobre, novembre, décembre 2008
doi: 10.1684/epi.2008.0194
E
´pilepsies 2008 ; 20 (4) : 220-8
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Experiments conducted in primates confirmed these observations -or showed primate specificities. Thus, while principal
glutamatergic and GABA interneurons originate from different primordia in mice, in primates, interneurones mostly
arise from contical ventricular zone, as glutamatergic neurons do. Differences in the kinetics of cell division in the
ventricular and subventricular cortical zone appear to control the expansion of the cerebral cortex and particularly of the
upper cortical layers in primates. The better knowledge of the mechanism of cerebral cortex development that we have
reached allows to understand better developmental disorders, from lamination defects to subtle disequilibrium in
cortical networks. Such, anomalies underlie several neuropsychiatric disorders, including epilepsy.
Key words:cerebral cortex, development, corticogenesis, lamination, axonal refinement
La mise en place du cortex cérébral est une opération com-
plexe qui met en jeu la production d’une variété remarquable de
neurones excitateurs et inhibiteurs (probablement plus d’une
centaine de types cellulaires distincts). Ces neurones sont ensuite
assemblés en circuits fonctionnels qui s’organisent en couches et
en régions, formant des aires corticales dont la fonction est très
variée, depuis les sensations élémentaires jusqu’à l’élaboration de
pensées abstraites. Cette complexité implique des ratés, et de fait,
les pathologies du développement cortical sont nombreuses et
variées ; elles jouent un rôle important dans l’étiologie de nom-
breuses pathologies neuropsychiatriques, en particulier dans
l’épilepsie. Dans certains cas, il s’agit de pathologies sévères de la
mise en place du cortex à des stades précoces du développement
comme des malformations et des désordres de lamination, mais
souvent il peut s’agir d’altérations plus subtiles de la formation et
du raffinement des connexions nerveuses qui altèrent la balance
excitation/inhibition. Le cortex a une expansion maximale chez
l’homme, où il représente une part importante du volume céré-
bral, mais les grands principes de son organisation sont conservés
chez tous les mammifères, depuis les rongeurs jusqu’aux primates.
Les modèles animaux, et en particulier les modèles issus des
approches génétiques chez la souris ont permis de faire un bond
remarquable dans nos connaissances au cours des dernières an-
nées, permettant de mieux comprendre les mécanismes des étapes
majeures du développement cortical. Ainsi, le travail de nombreu-
ses équipes dans le monde a permis de distinguer différentes
sources (provenances) de neurones corticaux, d’identifier les gè-
nes qui contrôlent leur spécification et leur migration ainsi que
des mécanismes qui permettent l’établissement des connexions
nerveuses et de cartes corticales fonctionnelles. Parallèlement aux
études sur le modèle souris, des explorations conduites chez les
primates, ont permis, de leur côté, de confirmer les observations
faites chez le rongeur, et aussi d’identifier des particularités du
développement cortical des primates, probablement liées à l’ex-
pansion particulièrement importante de cette structure dans cet
ordre mammalien. Sans pouvoir ici couvrir l’ensemble de ce
domaine très foisonnant, nous résumerons quelques unes des
principales étapes de ce développement, en mentionnant, quand
ces données existent, les particularités du développement cortical
chez l’homme.
Mise en place de l’ébauche corticale :
le télencéphale, le pallium et le subpallium
A des stades précoces de l’embryogenèse, le système ner-
veux central est constitué par un tube nerveux peu différencié,
formé par des cellules en prolifération qui constituent l’épithé-
lium ventriculaire. Assez rapidement, des mouvements mor-
phogénétiques modèlent ce tube neural en trois puis cinq
vésicules. La vésicule la plus antérieure est le télencéphale, qui
va donner naissance au cortex, qui va par la suite se diviser en 2
vésicules paires ; la troisième vésicule va former le diencéphale
qui produit entre autres, le thalamus, une structure étroitement
connectée au cortex (figure 1A, B). Dès la fermeture de la vésicule
télencéphalique, aux alentours de un mois chez l’homme (De-
trait et al., 2005), on distingue une partie dorsale du té-
lencéphale, appelée “palliale” (manteau en latin), et une partie
ventrale, appelée « sub-palliale » (figure 1B, C). Cette distinc-
tion, faite d’abord sur des critères morphologiques, correspond
à des entités neurogéniques différentes. Ainsi, l’expression des
gènes proneuraux se distribue différemment entre ces deux
territoires, qui vont donner, comme on le verra, des populations
neuronales distinctes. Ces gènes sont très conservés au cours de
l’évolution, et leur expression dans des domaines exclusifs
assure le maintien de l’identité des régions, et par extension
l’identité des neurones qui y sont produits. Par exemple le gène
« neurogenine » est exprimé dans le pallium, tandis que le gène
Mash1 est exprimé dans le subpallium. Ces gènes identifiés
initialement chez la drosophile (ath1, et ash1), ont des homo-
logues, chez l’homme, il s’agit respectivement de Hath1 et
Hash1 (Gradwohl et al., 1996 ; Ma et al., 1997 ; Ben-Arie et al.,
1996 ; de Pontual et al., 2003), le préfixe « H », désignant l’ho-
mologue humain.
Les neurones qui composent le cortex cérébral proviennent
de ces deux régions :
–
le pallium qui donne naissance à la majorité des structures
corticales (figure 1B). Les neurones issus de ces régions sont en
général glutamatergiques et ont une migration de type radial. La
région médiane de ce pallium devient l’hippocampe (archicor-
tex), la partie dorsale donne le cortex cérébral (le néocortex) et
la partie latérale se différencie en cortex limbique (paléocortex).
Le néocortex occupe la plus grande part du pallium. Il est
221 E
´pilepsies, vol. 20, n° 4, octobre, novembre, décembre 2008
Développement du cortex cérébral : apports récents des études chez la souris et les primates
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

caractérisé par une structure en six couches, tandis que l’archi-
cortex et le paléocortex ont des structures cellulaires relative-
ment plus simples, formées de 3 ou 4 couches ;
–
le subpallium qui est situé dans la partie ventrale du té-
lencéphale et comporte deux épaississements des parois du tube
neural. Il s’agit des éminences ganglionnaires latérales (EGL) et
médianes (EGM) (figure 1B). Ces structures génèrent des inter-
neurones de type GABAergique, dont le mode de migration est
tangentiel, c’est-à-dire qu’ils traversent des distances assez lon-
gues, avant de rejoindre leur localisation finale et de commen-
cer à se différencier. Les éminences ganglionnaires latérales
produisent les neurones du striatum et du pallidum, tandis que
les éminences ganglionnaires médianes et caudales produisent
les interneurones corticaux et hippocampiques (néocortex, ar-
chicortex et paléocortex).
Premiers stades de la neurogenèse corticale :
formation de la préplaque
Pendant une première période de 10 jours chez la souris, et
de1à2moischezl’homme, le neuroépithélium pallial a un
comportement purement prolifératif qui lui permet d’accroître
la surface globale du télencéphale et donc du futur cortex.
Pendant cette période, les progéniteurs se divisent de manière
symétrique, donnant deux progéniteurs qui sont eux- mêmes
capables de proliférer (Noctor et al., 2004). Ce mode de division
accroît de manière exponentielle le nombre de précurseurs
corticaux. Mais aucun neurone au sens strict, n’est produit à ce
moment là.
Aux alentours du 11
e
jour de vie embryonnaire chez la
souris, et de deux mois chez l’homme (Meyer et Wahle, 1999), le
neuroépithélium cortical opère une transition lui permettant de
produire les premiers neurones. C’est le début de la neuroge-
nèse. Les progéniteurs passent d’un mode prolifératif symétri-
que à un mode dit « asymétrique » où chaque division cellulaire
produit d’une part un progéniteur qui demeure dans le neuro-
épithélium, et un neuroblaste qui migre radialement hors de
l’épithélium ventriculaire, en se dirigeant vers la surface du
télencéphale. Cette première migration se fait sans support
glial, et forme l’ébauche corticale (figure 2A). (Noctor et al.,
2004 ; Kosodo et al., 2004 ; Shen et al., 2002). Ces neurones ne
sont en fait pas les premiers, car ils rejoignent, à la surface du
télencéphale, une population de neurones « précurseurs » que
sont les cellules de Cajal-Retzius. Les cellules de Cajal-Retzius
sont, quant à elles, générées à la périphérie du pallium dès le
jour embryonnaire 10 chez la souris (Bielle et al., 2005) et
migrent tangentiellement pour se positionner à la surface cor-
ticale lors de stades très précoces. Chez l’homme, une popula-
tion de neurones encore plus précoces a été récemment décrite.
Il s’agit de neurones « prédécesseurs » qui colonisent la surface
du neuroépithélium dès la fermeture du tube neural, au
30
e
jour de l’embryogenèse. Ces neurones n’ont jusqu’à présent
pas été identifiés dans d’autres espèces (Bystron et al., 2006).
C’est donc un ensemble de neurones hétérogènes s’assem-
blant en une première ébauche corticale qui constitue la « pré-
plaque ». La plupart des neurones de la préplaque disparaissent
par mort cellulaire programmée au cours de la maturation du
Tube neural à
trois vesicules
Tube neural à
cinq vesicules
Pallium
Cervelet
Cortex cérébral
Bulbe rachidien
Interneurones GABAergiques extrinsèques du cortex : 70%
Interneurones GABAergiques intrinsèques du cortex : 30%
Neurones glutamatergiques
Sub-pallium
Sub-pallium
Sub-pallium ZV
ZV
ZV
ZV
EGM
EGL
EGM
EGL
Proéncéphale
Télencéphale
Mésencéphale Cortex cérébral
Ventricule
Ventricule
Télencéphale humain
origine des neurones excitateurs
Télencéphale humain
origine des interneurones
Diencéphale
Diencéphale
Mésencéphale
Métencéphale
Myélencéphale
Rhombencéphale
Mésencéphale
AB
C
D
Figure 1
.
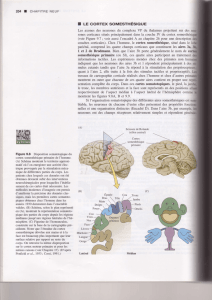
Développement de l’encéphale et origine des neurones du cortex cérébral. A) Au cours du développement précoce du système nerveux,
le tube neural se modèle en trois puis cinq vésicules préfigurant les grandes divisions de l’encéphale ; B) schéma de l’origine des neurones du
cortex cérébral humain. Les neurones du cortex cérébral ont deux origines, palliale et subpalliale, correspondant à deux compartiments du
télencéphale ; C) tous les neurones excitateurs, glutamatergiques, sont générés localement dans la zone proliférative palliale (ZV pour zone
ventriculaire) ; D) chez l’homme, les interneurones ont deux origines : 70 % d’entre eux ont, comme pour les neurones excitateurs, une origine
locale (D-droite), tandis que les 30 % restants ont une origine extrinsèque. Ils sont générés dans le sub-pallium, par les éminences ganglionnaires
latérales et médianes (EGL, EGM) et migrent tangentiellement pour rejoindre le cortex (D-gauche).
N. Narboux-Nême, P. Gaspar
222
E
´pilepsies, vol. 20, n° 4, octobre, novembre, décembre 2008
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

cortex cérébral. C’est le cas des cellules de Cajal-Retzius qui
meurent pendant la vie postnatale chez les rongeurs (del Rio et
al., 1995 ; Price et al., 1997), alors qu’une partie de ces neurones
survit chez l’homme. Quoi qu’il en soit, ces neurones « précur-
seurs » jouent un rôle fondamental au cours du développement
embryonnaire. En effet, la préplaque se comporte comme une
ébauche de cortex, facilitant les migrations cellulaires et l’éta-
blissement des projections axonales. Par exemple, les cellules de
Cajal-Retzius, régulent le positionnement des neurones corti-
caux dans l’épaisseur corticale en sécrétant une protéine de
matrice extracellulaire, appelée la « reelin » (D’Arcangelo et al.,
1995). D’autres neurones précurseurs pourraient servir de pion-
niers en envoyant des projections axonales longues vers le
cortex controlatéral, mais aussi vers des régions extra-corticales,
comme le thalamus, ou le tronc cérébral. Ces projections préco-
ces immatures pourraient servir de guide pour les neurones
corticaux suivants (De Carlos et O’Leary, 1992 ; McConnell et
al., 1989). Réciproquement, les cellules de la préplaque guident
les axones d’origine extra-corticale vers leurs cibles spécifiques
dans le cortex cérébral (Molnár et Blakemore, 1995 ; Shimogori
et Grove, 2005). Des interactions entre les axones thalamo-
corticaux et des axones cortico-thalamiques en développement
pourraient ainsi contribuer à guider ces projections vers leur
cible spécifique (Molnár et Blakemore, 1995).
Après la mise en place de la préplaque commence une
période de production de neurones de la plaque corticale, et de
migration des interneurones, qui formeront ensemble les cir-
cuits fonctionnels du cortex mature. Les vagues successives des
nouveaux neurones (voir paragraphe suivant) s’intercalent au
milieu des neurones de la préplaque, la scindant en deux par-
ties, une zone marginale en surface, et la sous-plaque près de la
zone ventriculaire (figure 2B). Au terme du développement, les
reliquats de la zone marginale deviendront la couche I du cortex
cérébral, très pauvre en corps cellulaires, tandis que certains
neurones survivants de la sous-plaque intégreront la partie
ventriculaire de la couche la plus basale, la couche VIb (Heuer
et al., 2003).
Les progéniteurs basaux
Au cours de la corticogenèse, les étapes d’amplification des
progéniteurs jouent un rôle important pour déterminer le nom-
bre de neurones adultes dans chaque couche. Récemment il a
PP
n
cgr ZV
pb
ZV
SP
PC
ZM
ZV
SP
PC
ZM
ABC
Figure 2
.
Schéma de génération des neurones excitateurs au cours de la corticogenèse. A) Les cellules de la glie radiaire (cgr) de la zone
ventriculaire corticale (ZV) produisent les premiers neuroblastes (n) qui forment la préplaque (PP) ; B) Les neurones de la plaque corticale (PC)
sont générés dans un second temps. Les neuroblastes des couches corticales migrent sur le support de la glie radiaire pour se positionner au milieu
de la préplaque, qui est scindée en deux régions : la zone marginale en surface (ZM) et la sous-plaque (SP) ; C) Les neurones des couches
corticales sont générés successivement, des couches profondes aux couches superficielles. Au lieu de produire un neuroblaste, les cgr peuvent
générer un progéniteur basal (pb) capable de se diviser en au moins deux neuroblastes.
223 E
´pilepsies, vol. 20, n° 4, octobre, novembre, décembre 2008
Développement du cortex cérébral : apports récents des études chez la souris et les primates
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

été montré, qu’en plus de l’amplification des progéniteurs dans
l’épithélium ventriculaire, discutée précédemment, il y avait
une amplification de certains neuroblastes. Ainsi, à la suite
d’une division asymétrique, le progéniteur cortical peut pro-
duire un progéniteur détaché du neuroépithélium avec des
propriétés limitées de prolifération. Typiquement, ces progéni-
teurs détachés ne peuvent se diviser qu’une fois (figure 2B, C).
Ces progéniteurs basaux existent chez la souris comme chez
l’homme où ils peuvent être suivis par des marqueurs spécifi-
ques (tbr2) (Haubensak et al., 2004 ; Carpenter et al., 2001), mais
dans des proportions différentes. Il semble que ce soit par la
modulation de cette étape d’amplification que le cortex cérébral
humain acquière une telle expansion de sa surface au cours de
l’évolution, sans commune mesure avec l’augmentation de
taille des autres régions du système nerveux central (Finlay et
Darlington, 1995).
Formation de la plaque corticale, les neurones principaux
des couches du cortex cérébral
Les neurones excitateurs, glutamatergiques, du cortex céré-
bral sont produits localement dans la zone ventriculaire corti-
cale (Mione et al., 1997). Ils sont à la base de la communication
rapide à courte et longue distance dans le cortex cérébral. Ces
neurones migrent radialement à partir de la zone ventriculaire,
impliquant des interactions étroites avec la glie radiaire (Nada-
rajah et al., 2001). Les neurones des couches profondes sont les
premiers produits, tandis que les neurones les plus superficiels
sont les plus jeunes. Dans les couches intermédiaires, les neuro-
nes suivent globalement la règle selon laquelle plus ils sont
générés tard, plus ils sont localisés superficiellement, avec un
patron « inside-out » (figure 2C ; Angevine et Sidman, 1961 ;
McConnell, 1988). Les neurones produits dans la région ventri-
culaire migrent vers la surface piale, guidés par le prolongement
de leur cellule mère, une cellule de glie radiaire (Malatesta et al.,
2000 ; Noctor et al., 2001). Les cellules de la glie radiaire sont en
fait à la fois des précurseurs et des guides, elles génèrent les
neuroblastes tout en leur servant de guide pour se positionner
en colonnes dans l’épaisseur corticale. Ce rôle prend tout son
sens chez l’homme, où la déformation de la surface corticale par
la formation de sillons et de circonvolutions complique la
trajectoire de migration des neurones (Rakic, 1974). Des expé-
riences de greffes hétérochroniques de progéniteurs corticaux
dissociés chez la souris ont montré que l’identité de couche
corticale est acquise à un moment précis du cycle cellulaire,
mais aussi qu’il existe une horloge cellulaire interdisant la
génération du type de neurones déjà produits. Ceci permet de
restreindre progressivement la multipotence des progéniteurs
corticaux (McConnell et Kaznowski, 1991 ; Desai et McConnell,
2000 ; Frantz et McConnell, 1996). Récemment des études faites
à partir de cellules souches embryonnaires, ont montré, qu’in
vitro il était possible de reproduire cette séquence d’émergence
de différentes catégories de neurones corticaux (Gaspard et al.,
2008).
La migration radiaire, conduit les jeunes neuroblastes à se
positionner à la surface de la plaque corticale, formant une
structure dense, composée de neuroblastes récemment pro-
duits, et encore peu différenciés. Ce n’est que dans un second
temps, après un délai nécessaire pour « sortir » de la plaque
corticale, que les neurones corticaux prennent leur place défi-
nitive dans l’épaisseur corticale (Boulder Committee, 1970 ;
Bayer et Altman, 1991). Chez l’homme, ces migrations radiaires
connaissent un pic entre les troisième et sixième mois de gros-
sesse, et se terminent au cours du troisième trimestre de la
grossesse (Sidman et Rakic, 1973 ; Rakic et al., 1994 ; Gressens,
2000). Ce n’est qu’à partir du septième mois de grossesse que
l’on peut observer clairement sur le plan structural l’organisa-
tion caractéristique en six couches du neocortex (Chenn et al.,
1997 ; Chan et al., 2002).
Les interneurones du cortex cérébral
Les interneurones constituent environ 20 % des neurones
du cortex, ils ont une fonction inhibitrice essentielle dans la
mise en place de circuits neuronaux fonctionnels. Les interneu-
rones corticaux constituent une population très hétérogène :
des catégories d’interneurones se distinguent par leur morpho-
logie, leur localisation, ou encore sur la base de leur profil
d’expression protéique, et de leurs propriétés physiologiques
(DeFelipe, 1997). De fait nombre d’interneurones sont capables
de produire et de libérer des neuropeptides en plus du GABA,
permettant une modulation de l’activité des circuits. Contraire-
ment aux neurones excitateurs, les interneurones ont une ori-
gine extrinsèque chez les rongeurs. Ils sont principalement
générés au niveau des éminences ganglionnaires, dans le sub-
pallium, et ils colonisent l’ébauche corticale par migration
tangentielle à longue distance depuis cette région (figure 1D
gauche, Anderson et al., 1997). Cette migration dépend de
nombreux facteurs intrinsèques (motilité des neurones) et ex-
trinsèques (molécules de guidage), et elle est perturbée dans
différentes mutations responsables de syndromes épileptiques.
Par exemple la perte de fonction de la protéine double cortine
(cause de retard mental avec épilepsie chez l’homme) provoque
des anomalies caractéristiques de la migration des interneuro-
nes corticaux (Leger et al., 2008).
Il existe cependant une particularité de la production des
interneurones chez les primates. Chez le singe, les interneuro-
nes d’origine extrinsèque ne représentent que 30 % des inter-
neurones corticaux (Letinic et al., 2002). Les autres sont générés
localement par le neuroépithélium cortical (figure 1D, droite).
De manière intéressante c’est une possibilité qui existe aussi
chez la souris dans certaines conditions expérimentales (Gulacsi
et Lillien, 2003, Anderson et al., 1999 ; Bellion et al., 2003), mais
qui est vraisemblablement inhibée in vivo chez les rongeurs. La
singularité de l’origine des interneurones pourrait avoir été
sélectionnée par l’évolution pour s’adapter à la gigantesque
augmentation de la surface palliale qui est beaucoup plus im-
portante proportionnellement que l’augmentation de la taille
des zones sous-palliales (source habituelle des interneurones
dans les autres espèces).
N. Narboux-Nême, P. Gaspar
224
E
´pilepsies, vol. 20, n° 4, octobre, novembre, décembre 2008
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%