HYPERSENSIBILITE DUE AUX COMPLEXES IMMUNS : HS III

HYPERSENSIBILITE DUE AUX COMPLEXES
IMMUNS : HS III
I/ INTRODUCTION
II/PRESENTATION DES COMPLEXEXS IMMUNS CIRCULANTS
III/PATHOLOGIES DES COMPLEXES IMMUNS FORMES IN
SITU
IV/PHATHOLOGIES DES COMPLEXES IMMUNS CIRCULANTS
V/ MECANISMES DE L’ACTION PATHOGENE DES
COMPLEXES IMMUNS
VI/ DETECTION DES COMPLEXES IMMUNS
Dr:Y.Bouchedoub

INTRODUCTION
•Ces réactions sont la conséquence de la localisation
des complexes Ag-Ac à l’intérieur et autour des petits
vaisseaux sanguins avec comme conséquence
principale une inflammation de ces vaisseaux, il en
résulte une diminution de la circulation dans les tissus
adjacents.
•Le phénomène d’Arthus et la maladie sérique aigue
constituent deux modèles expérimentaux classiques de
cette réaction.
•Les maladies liées à une HS III sont essentiellement la
maladie sérique et les alvéolites extrinsèques.

INTRODUCTION
•De nombreux complexes immuns se forment en
permanence dans l’organisme, ces complexes sont
normalement éliminés par le système des phagocytes
mononuclées du foie de la rate et du poumon et des autres
organes.
•Parfois la formation de complexes immuns peut entraîner
des lésions surtout vasculaires au cours de certaines
maladies (infectieuses, auto-immunes, ou allergiques).
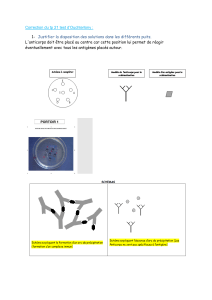
•Contrairement aux manifestations de l’allergie immédiate
qui nécessitent une sensibilisation préalable par l’allergène
pour apparaître. Une réaction d’hypersensibilité type III
peut survenir dés le premier contact avec l’antigène

Présentation des complexes immuns circulants
•Les complexes immuns circulants (CIC) ou immuns complexes,
sont des associations macromoléculaires résultant d’une
interaction antigène-anticorps. formés lors de toute réponse
anticorps à une immunisation, dans le but d’éliminer la substance
reconnue.
Deux types d’immuns complexes se distinguent selon les quantités
en antigène et en anticorps qu’ils contiennent.
•Les complexes formés en excès d’anticorps, sont peu solubles et
leur élimination est facilitée par les cellules du système mono-
macrophagique.
•Les complexes formés en excès d’antigène, sont solubles,
difficilement captés par les macrophages pouvant dans certaines
circonstances se déposer au niveau de l’endothélium vasculaire et
provoquer des lésions

Présentation des complexes immuns circulants
Ces complexes immuns peuvent impliquer deux types
d’antigènes :
•Des antigènes exogènes : microorganismes entiers,
toxines, virus, allergènes, antigènes alimentaires.
•Des antigènes endogènes : ADN, immunoglobulines
(facteur rhumatoïde), enzymes, protéines circulantes.
Au cours de la réponse immunitaire, les complexes
immuns sont d’abord formés d’un excès d’antigène,
puis la concentration en anticorps augmente.
Deux éléments interviennent dans l’élimination des
complexes immuns circulants :
•Le complément et les récepteurs CR1
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
1
/
27
100%