Post-Chicago 2013

La Lettre du Cancérologue
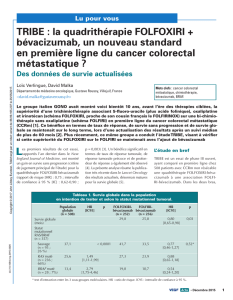
TRIBE : FOLFOXIRI-bévacizumab
versus FOLFIRI-bévacizumab (1)
Objectif principal : survie sans progression (HR : 0,75)
ASCO®2013 - D'après Falcone A et al., abstr. 3505, actualisé
07/08-05/11 :
504 patients
- CCRm non
résécable
- 1re ligne
- OMS 0-2
(0 si 71-75 ans)
FOLFOXIRI + bévacizumab
Bévacizumab 5 mg/kg, irinotécan 165 mg/m2,
oxaliplatine 85 mg/m2, LV 200 mg/m2,
5FU 3 200 mg/m2sur 48 h, J1 = J15
(n = 250)
FOLFIRI + bévacizumab
Bévacizumab 5 mg/kg, irinotécan 180 mg/m2,
LV 200 mg/m2, 5FU bolus 400 mg/m2,
5FU 2 400 mg/m2sur 48 h, J1 = J15
(n = 254)
R
12 cycles
puis relais
par 5FU +
bévacizumab
jusqu'à
progression
Essai de phase III italien du GONO

La Lettre du Cancérologue
TRIBE : FOLFOXIRI-bévacizumab
versus FOLFIRI-bévacizumab (2)
FOLFOXIRI +
bévacizumab
(n = 250)
FOLFIRI +
bévacizumab
(n = 254)
Sexe masculin (%) 60 61
Âge médian (ans) 61 60
OMS 0/1-2 (%) 90/10 89/11
Métastases synchrones (%) 79 81
Chimiothérapie adjuvante (%) 12 12
Nombre de sites métastatiques (1/>1)
[%] 31/69 24/76
Métastases hépatiques exclusives (%) 23 18
Primitif réséqué (%) 69 65
Score de Köhne
(faible/intermédiaire/élevé/ND) [%] 43/44/7/6 41/44/11/4
Caractéristiques des patients
ASCO®2013 - D'après Falcone A et al., abstr. 3505, actualisé

La Lettre du Cancérologue
TRIBE : FOLFOXIRI-bévacizumab
versus FOLFIRI-bévacizumab (3)
FOLFOXIRI +
bévacizumab
(n = 250)
FOLFIRI +
bévacizumab
(n = 254)
Effets indésirables sévères (%) 20,4 19,7
Effets indésirables fatals (%) 2,8 3,5
Décès liés au traitement (%) 2,4 1,6
Décès précoces (60 jours) [%] 3,2 2,3
Tolérance
ASCO®2013 - D'après Falcone A et al., abstr. 3505, actualisé
•Augmentation significative des diarrhées, des mucites, de la neuropathie
et de la neutropénie
•Pas d’augmentation des neutropénies fébriles
•Pas d’augmentation des effets indésirables imputables au bévacizumab

La Lettre du Cancérologue
TRIBE : FOLFOXIRI-bévacizumab
versus FOLFIRI-bévacizumab (4)
0 6 12 18 24 30 36 42 48
0
20
40
60
80
100
Probabilité d’absence de progression
54 60
FOLFIRI + bévacizumab
FOLFIXIRI + bévacizumab
Suivi médian : 32,3 mois
FOLFIRI + bévacizumab
226 événements
FOLFOXIRI + bévacizumab
213 événements
Médianes
FOLFIRI + bévacizumab : 9,7 mois
FOLFOXIRI + bévacizumab : 12,1 mois
HR non stratifié = 0,77 (0,64-0,93)
p = 0,006
Mois
Survie sans progression
ASCO®2013 - D'après Falcone A et al., abstr. 3505, actualisé

La Lettre du Cancérologue
TRIBE : FOLFOXIRI-bévacizumab
versus FOLFIRI-bévacizumab (5)
0 6 12 18 24 30 36 42 48
0
20
40
60
80
100
Probabilité d’absence de progression
54
Suivi médian : 32,3 mois
FOLFIRI + bévacizumab : 155/256 décédés
FOLFOXIRI + bévacizumab : 131/252 décédés
Médianes :
FOLFIRI + bévacizumab : 25,8 mois
FOLFOXIRI + bévacizumab : 31,0 mois
HR non stratifié = 0,83 (0,66-1,05) ; p = 0,125
HR stratifié = 0,79 (0,63-1,00) ; p = 0,054
Mois
Survie globale (données non matures)
ASCO®2013 - D'après Falcone A et al., abstr. 3505, actualisé
FOLFIRI + bévacizumab
FOLFIXIRI + bévacizumab
 6
6
1
/
6
100%