Echanges plasmatiques et Ig IV dans la prise en charge des

Plasmaphérèse
Syndrome de Guillain Barre
Myasthénie
DESC Réanimation Médicale
Juin 2008
IgIV
SUSSET Vincent
POROT Véronique

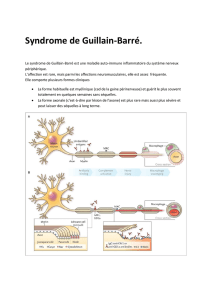
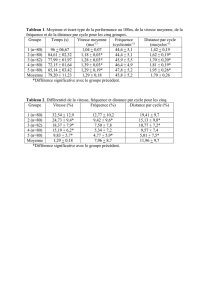
Syndrome de Guillain Barré
1,3 à 2 / 100000 / an
Recours à la ventilation mécanique dans 25% des cas
Mortalité entre 4 et 15 %
Van Koningsveld et al., 2000; Govoni and Granieri, 2001
Neuropathie aiguë à prédominance motrice avec paralysie
d’évolution ascendante
PL: Dissociation albumino-cytologique
Plusieurs entités cliniques distinctes (AMAN, ASMAN)
Risque vital mis en jeu par l’extension aux muscles
respiratoires de la paralysie, la dysautonomie, les
complications thrombo-emboliques ou infectieuses
Séquelles motrices 20%, fatigue persistente 67%

Physiopathologie
Facteur déclenchant retrouvé dans 2/3 des cas: Infections
à Campylobacter jejuni, CMV, EBV, Mycoplasma pneumoniae, HIV, VZV,
haemophilus influenzae
Réaction auto-immune 1 à 4 semaines après
Atteinte démyélinisante prédominant aux racines des nerfs
périphériques
Immunité cellulaire: Infiltration lymphocytaire des gaines
de myéline, éventuellement infiltration axonale
macrophagique
Intérêt théorique des corticoïdes (échec démontré /
6 essais thérapeutiques )
Immunité humorale: complément, anticorps dirigés contre
des gangliosides constitutifs de la myéline, cytokines
Intérêt théorique des EP et des IgIV

J 0
Récupération
Déficit
moteur
Extension
Plateau
Temps
Evénements
prodromiques
Séquelles
Mesures symptomatiques
Mesures spécifiques associées aux précédentes
diminuer la gravité et la durée de la phase aiguë
diminuer la fréquence
des séquelles
Principes de prise en charge

Echanges plasmatiques
consiste à remplacer le plasma du patient par une solution
permettant de maintenir une pression oncotique équivalente
solution de remplacement: PFC (plasma frais congelé) ou
albumine 4% ou colloïdes
•épurer le plasma de molécules trop grosses pour être
éliminées à travers des membranes d'hémodialyse ou des
filtres d'hémofiltration traditionnels notamment des auto-
anticorps ou des complexes immuns circulants
•amélioration du système réticulo-endothélial
•ou dans le cas du purpura thrombotique thrombocytopénique
par le remplacement de facteurs postulés déficients par
l'administration de PFC
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
1
/
78
100%