Place du médecin traitant dans la prise en char

Place du médecin traitant dans la prise en charge de la
Dégénérescence Maculaire liée à l’Âge (DMLA).
L.MAHIEU
La DMLA est devenue est un problème de santé publique avec un sujet atteint sur 10 après 80
ans. Sa fréquence augmente avec l’âge et l’allongement de l’espérance de vie dans nos pays
laisse augurer un nombre croissant de patients à prendre en charge. C’est, en effet, la
principale cause de malvoyance dans les pays industrialisés.
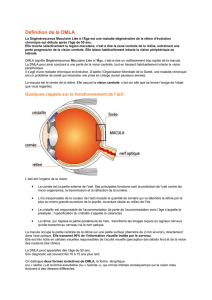
I. Définition
Le terme de dégénérescence maculaire liée à l’âge fait référence à une définition ancienne
d’une « lésion de la région maculaire, dégénérative, non inflammatoire »; or des découvertes
récentes ont impliqué des phénomènes inflammatoires ainsi que des facteurs de prédisposition
génétiques. On pourrait donc définir la DMLA comme une atteinte maculaire tardive,
multifactorielle, apparaissant sur un terrain génétiquement prédéterminé, dont
l’expression clinique est fonction de facteurs additionnels et environnementaux.
Cliniquement, elle associe diversement des anomalies de l’épithélium pigmentaire et de la
rétine sensorielle et/ou des drusen et des néovaisseaux sous-rétiniens. On distingue 2 stades
évolutifs :
- un stade initial de maculopathie liée à l’âge (MLA) = formes débutantes
caractérisées par des remaniements de l’épithélium pigmentaire et des dépôts sous-
rétiniens appelés drusen
- un stade avancé de dégénérescence maculaire liée à l’âge proprement dite
(DMLA) = formes tardives correspondant aux complications atrophiques (forme
« sèche ») et néovasculaires (forme « humide »). La forme atrophique « sèche » est
une atrophie progressive des différentes couches cellulaires (épithélium pigmentaire,
photorécepteurs et choriocapillaire). La forme exsudative « humide » est une
prolifération anormale de vaisseaux néoformés sous la rétine à partir de la
vascularisation choroïdienne. Ces néovaisseaux choroïdiens (NVC) laissent diffuser
sous et dans la rétine du sang et des fluides qui sont à l’origine des troubles visuels.
Cette accumulation de fluides explique la terminologie de forme « humide ». Ces 2
formes (atrophique et exsudative) conduisent inéluctablement à la destructions des
photorécepteurs maculaires et la perte de la vision centrale.
II. Physiopathologie multifactorielle
1. L’âge
L’âge est un facteur fondamental. En effet, les fonctions de transport (fluides, acides aminés,
métabolites) entre la rétine et la choriocapillaire diminue avec l’âge. Ce déclin fait partie du
vieillissement normal, mais est accéléré dans la DMLA sous l’effet de gènes régulateurs. Des
modifications anatomiques se produisent également lors du vieillissement rétinien
principalement au niveau de la rétine externe, de l’épithélium pigmentaire et de la membrane
de Bruch aboutissant à un épaississement de la membrane de Bruch. Puis lorsque le
déséquilibre entre production de débris métaboliques par la rétine externe et élimination de
ces débris par l’épithélium pigmentaire s’accroît, ces débris s’accumulent formant de
véritables dépôts sous-rétiniens appelés drusen. Ces dépôts eux-mêmes vont gêner les
mécanismes de transport.

2. Le stress oxydatif
Le métabolisme rétinien élevé libère des espèces oxygénées réactives (EOR). Ces molécules
hautement réactives peuvent endommager par oxydation les protéines, les acides nucléiques et
les lipides, entraînant des dommages cellulaires. La rétine, riche en chromophores et en acides
gras polyinsaturés, est particulièrement sensible aux réactions d’oxydation. Les mécanismes
de défense antioxydants agissent par l’intermédiaire d’enzymes (ex : superoxyde dismutase)
et de composés non enzymatiques provenant principalement de l’alimentation, tel que les
vitamines C et E, les caroténoïdes ou le zinc. La diminution des antioxydants et
l’augmentation des pro-oxydants avec l’âge associée à la réduction du pigment maculaire, et
le rôle néfaste du tabagisme sont autant d’arguments pour conforter le rôle du stress oxydatif
dans la DMLA. L’étude AREDS (Age-related Eye Disease Study, étude prospective,
randomisée, et contrôlée) a démontré l’efficacité de l’administration systémique préventive
d’antioxydants dans la DMLA. Une supplémentation orale en pigment maculaire (lutéine et
zéaxanthine) est également possible car un faisceau d’arguments reposant sur des données
épidémiologiques, expérimentales et cliniques, suggère un rôle préventif du pigment
maculaire dans la DMLA.
3. Facteurs génétiques
Plusieurs gènes ont été identifiés comme facteurs protecteurs ou prédisposant de la DMLA.
Actuellement cinq gènes ont été mis en évidence, qui expliquerait l’atteinte de près de la
moitié des patients :
ApoE (apolipoprotéine E) : rôle protecteur de l’allèle ε4 vis-à-vis DMLA
ABCA4 : 2 mutations facteurs de susceptibilité prédisposant à la DMLA
CFH (facteur H du complément) : rôle prédisposant de l’allèle C
CFB (facteur B du complément) : rôle protecteur de certains polymorphismes
LOC387715 : allèle de prédisposition
III. Symptomatologie
Trois signes doivent alerter le patient et ses médecins sur l’existence d’une probable DMLA.
Il s’agit :
- d’une baisse d’acuité visuelle (surtout si elle est rapidement progressive et unilatérale)
- de métamorphopsies (déformations des images perçues par le patient)
- d’un scotome (tache +/- opaque dans la partie centrale du champ visuel)
1. Signes fonctionnels au stade de MLA
La baisse d’acuité visuelle est souvent minime ou modérée aux stades débutants avec une
sensation de brouillard, et de gêne visuelle prédominant à la lecture. Il existe également une
modification du sens chromatique (jaunissement des couleurs), mais qui est rarement signalée
par les patients en dehors de ceux pratiquant la peinture. Il y a en outre un retard d’adaptation
à l’obscurité. L’ensemble de ces troubles amène les patients à augmenter le niveau
d’éclairement pour pouvoir lire. Néanmoins, à ce stade, les patients sont peu inquiets
attribuant souvent leur gêne à un début de cataracte.
2. Signes fonctionnels au stade de DMLA atrophique
Dans la forme sèche de la DMLA, la baisse d’acuité visuelle est lentement progressive avec
initialement peu de retentissement, puis entraînant progressivement une gêne croissante à la
lecture liée aux scotomes péricentraux (fatigue visuelle, augmentation de l’éclairage). Ces
scotomes sont rarement bien analysés par les patients qui se plaignent seulement de difficultés

visuelles. Au stade ultime, l’atrophie englobe le point de fixation aboutissant à un scotome
central et une baisse d’acuité visuelle majeure.
3. Signes fonctionnels au stade de DMLA exsudative
La forme exsudative de la DMLA se caractérise par un « syndrome maculaire » qui associe :
- une baisse d’acuité visuelle de près et de loin,
- des métamorphopsies (déformations des images)
- un trouble de la vision des couleurs et des contrastes
- un scotome relatif puis absolu
IV. Rôle du médecin traitant
1. Prévention primaire
Ensemble des actes destinés à diminuer l'incidence d'une maladie, donc à réduire l'apparition des nouveaux cas.
En agissant en amont cette prévention empêche l'apparition des maladies, elle utilise l'éducation et l'information
auprès de la population.
Le médecin traitant est parmi les professionnels de santé celui qui connaît souvent le mieux le
patient, ses antécédents, son cadre de vie et ses habitus. Il est donc le plus à même de repérer
les patients à risque de développer une DMLA :
- Antécédents familiaux de DMLA
- Tabagisme
- Alimentation mal équilibrée.
Le rôle du médecin traitant sera alors de proposer un arrêt du tabagisme, et une modification
du régime alimentaire favorisant les fruits, les légumes et les poissons.
2. Prévention secondaire
Ensemble d'actes destinés à diminuer la prévalence d'une maladie, donc à réduire sa durée d'évolution.
Intervient dans le dépistage de toutes les maladies et comprend le début des traitements de la maladie.
Chez tout patient présentant des facteurs de risque, ou se plaignant de troubles visuels, le rôle
du médecin traitant sera de proposer une consultation chez un ophtalmologiste (le degré
d’urgence du rendez-vous dépendant de la symptomatologie du patient). L’apparition récente
d’un syndrome maculaire doit par exemple amener à une consultation ophtalmologique en
urgence. Lorsque le médecin ophtalmologiste confirme la présence d’une MLA, une
supplémentation par vitamines et antioxydants au long cours sera proposée au patient.
3. Prévention tertiaire
Ensemble des actes destinés à diminuer la prévalence des incapacités chroniques ou des récidives dans la
population, donc à réduire les invalidités fonctionnelles dues à la maladie. Agit en aval de la maladie afin de
limiter ou de diminuer les conséquences de la maladie et d'éviter les rechutes. Dans ce stade de prévention les
professionnels s'occupent de la réeducation de la personne et de sa réinsertion professionnel et sociale.
Le dépistage précoce des complications néovasculaires (forme humide ou exsudative) ou de
leur récidive est essentiel pour limiter les conséquences visuelles. En effet, l’introduction des
injections intravitréennes d’anti-VEGF (le VEGF est le facteur de croissance principal des
néovaisseaux) a révolutionné le pronostic des formes exsudatives en stabilisant la vision de
90% des patients. D’où la nécessité de consulter le plus tôt possible avant que l’acuité visuelle
ne se soit effondrée. L’auto-surveillance hebdomadaire œil par œil avec une grille d’Amsler
(ou à défaut avec une grille de mots croisés ou une grille de sudoku) à la recherche de
déformation ou de scotomes est donc nécessaire. Le rôle du médecin traitant sera de rappeler
et de réexpliquer l’importance de l’autosurveillance ; la motivation des patients ayant
tendance à baisser avec le temps. Enfin lorsque malheureusement la malvoyance s’est
installée, une prise en charge sociale est souvent nécessaire (aide à domicile, prestation de

compensation du handicap …etc…). L’ensemble de ces demandes est habituellement réalisé
autour du patient par la famille et le médecin traitant.
1
/
4
100%