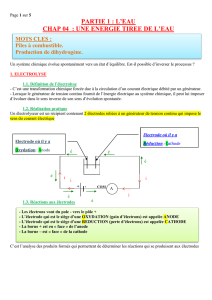
15 – Électrolyse

10 électrolyse
Plan détaillé
A – exemples d’électrolyse
1 – définition
On nomme électrolyse toute décomposition chimique produite par le courant
électrique. Les corps électrolysables, ou électrolytes, sont les acides, les
bases et les sels dissous ou fondus.
1 2 – étude du phénomène fondamental
a – Électrolyse du chlorure cuivrique
b – Interprétation de l’électrolyse
c – Nature du courant dans les électrolytes
3 – généralisation :
théorie des ions
Lorsqu’un acide, une base ou un
sel est en solution dans l’eau, ses
molécules sont dissociées en
ions : l’anion, qui porte une
charge électrique négative, et le
cation, qui porte une charge
positive.
● acide HA → H+ + A-
● base MOH → M+ + OH-
● sel MA → M+ + A-
4 – lois qualitatives de
l’électrolyse
● 1re loi.- Les produits de
l’électrolyse apparaissent au
voisinage des électrodes.
● 2e loi.- La réaction
chimique qui a lieu à l’anode

libère des électrons : c’est une oxydation.
La réaction chimique qui a lieu à la cathode consomme des
électrons : c’est une réduction.
● 3e loi.- L’oxydation anodique libère exactement autant
d’électrons qu’en consomme la réduction cathodique.
5 – exemple d’électrolyse simple
Électrolyse d’une solution de HCl :
6 – électrolyses complexes
a – Cations provenant de métaux très réducteurs
, :
b – Anions complexes stables (
) en présence d’une anode passive
:
c – Anode soluble
d – Décharge d’un ion complexe donnant un radical instable
Conclusion : En présence d’électrodes passives, certains ions complexes
(
,) se déchargent en donnant des composés instables, qui se
décomposent. On dit qu’il se produit une réaction secondaire.
e – Réactions entre les produits de l’électrolyse
( ) eau de javel.

B – étude quantitative
2 1- lois de Faraday
a – 1re loi
● Expérience
● Énoncé
b – 2e loi
● Expérience
● Énoncé
c – 3e loi
● Expérience
● Énoncé
3 2 – résumé des lois : formule
C – applications de l’électrolyse
1 – électrochimie
Elle décrit les relations mutuelles de la chimie et de l’électricité ou, mieux, des
phénomènes couplés à des échanges d’énergie électrique.
2 – électrométallurgie
a – Préparation des métaux
b – Affinage des métaux
3 – galvanoplastie
a – Dépôts galvaniques
b – Moulages galvaniques
dépôts et moulages galvaniques
Michael FARADAY
(1791 – 1867)

Questions développées
1 étude du phénomène fondamental
a – Électrolyse du chlorure cuivrique
Dans une cuve en U contenant une solution de chlorure
cuivrique CuCl2, plongeons deux électrodes de charbon
respectivement reliées aux pôles d’un générateur.
Fermons l’interrupteur de façon à faire passer le courant,
nous observons :
− un dépôt rougeâtre sur la cathode : c’est du cuivre;
−un dégagement de gaz sur l’anode. Le gaz dégagé est reconnaissable à
son odeur et à sa couleur : c’est du chlore.
b – Interprétation de l’électrolyse
En solution, les édifices du chlorure
cuivrique se dissocient en donnant deux
sortes d’ions qui se dispersent parmi les
molécules d’eau.
− Un ion Cu2+ est un atome de cuivre
dépourvu de deux électrons; de ce fait, il
porte deux charges positives 2e+ : c’est
le cation.
− Un ion Cl− est un atome de chlore
possédant, au contraire, un électron supplémentaire; il est par suite porteur
d’une charge négative e− : c’est l’anion.
La solution de chlorure cuivrique est électriquement neutre puisqu’elle
contient autant d’ions cuivrique Cu2+ que d’ions chlorure Cl− :
CuCl2 Cu2+ 2Cl− .
Dès la fermeture du circuit, les ions sont soumis à des forces électriques qui
les mettent en mouvement;
● A l’anode, les ions chlorure Cl− s’oxydent : chacun d’eux cède à l’anode
son électron excédentaire, se transformant ainsi en un atome de chlore, puis
ces atomes s’unissent deux à deux pour former les molécules diatomiques
Cl2 du chlore gazeux dont nous avons observé le dégagement sur l’anode.
Cet ensemble de transformations se résume par l’équation chimique :
2Cl− Cl2 2e−
● A la cathode, se produit la réduction des ions cuivriques Cu2+. Chacun
d’eux fixe deux électrons cédés par la cathode pour se transformer en atome
de cuivre métallique dont nous avons observé le dépôt sur la cathode.
Cet ensemble de transformations se résume par l’équation chimique :
Cu2+ 2e− Cu .

Dans tous les cas, le nombre des
électrons aspirés sur l’anode pendant un
certain temps est égal au nombre des
électrons cédés par la cathode dans le
même temps.
c – Nature du courant dans les
électrolytes
Dans la solution de chlorure cuivrique,
comme dans tout électrolyte, une double
migration, en sens inverse, d’anions et de
cations permet le passage du courant.
2 – lois de Faraday
a – Première loi-
●● Expérience.- Plaçons en série (à la suite les unes des autres, dans le
même circuit) plusieurs cuves
contenant de l’eau acidulée et
des électrodes inattaquables. La
forme des cuves est différente
ainsi que la forme, la surface et
la distance des électrodes.
Établissons le courant pendant
un certain temps : nous
constatons qu’à chaque instant,
et quelle que soit la durée de l’expérience, les volumes d’hydrogène dégagé
sur les cathodes sont égaux.
Nous ferions la même constatation pour les masses d’argent ou de cuivre
déposées dans des cuves à nitrate d’argent ou à sulfate de cuivre placées en
série.
● Énoncé.-
La masse d’un produit libéré sur une électrode, en un temps donné, est
indépendante des caractéristiques physiques et géométriques de la
cuve, des électrodes et de la solution.
b – Seconde loi ●
● Expérience.- Si, dans une des expériences précédentes, nous doublons,
triplons … l’intensité du courant, pour la même durée, nous constatons que la
masse de substance qui apparait à l’une des électrodes, est doublée,
triplée…
Donc : La masse de produit libéré à la cathode est proportionnelle à l’intensité
du courant. m = k ٠ I.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%