Mise en culture des cellules cérébrales embryonnaires de

Guillou Noëlline TP de culture cellulaire Chateigner Aurélien
1
TP de culture cellulaire
I. Introduction
Aujourd’hui, l’embryologie est une science qui s’est tournée vers la compréhension des mécanismes
qui permettent le développement des organismes. Pour la plupart des oiseaux, et notamment pour
notre poule, le développement de l’embryon se fait en dehors de l’organisme maternel, à l’abri d’une
protection, vulgairement appelée œuf.
Cet œuf contient toutes les ressources nécessaires au développement de l’embryon, que ce soit au
niveau de l’énergie, de l’eau et de la protection. L’enveloppe externe de cet embryon permet donc la
protection de l’embryon, de par sa composition en 3 parties principales : Vitellus, Amnios et
Allantoïde. Nous verrons les rôles de ces enveloppes dans la première partie.
En ce qui concerne le développement de l’embryon en lui-même, un certain nombre de processus se
mettent en place, que ce soit pour la division cellulaire en elle-même, ou pour la reconnaissance, la
migration et la différenciation cellulaire. Ces mécanismes ont pour finalité de former les tissus et les
organes de la future poule.
Composant ces tissus et organes, un grand nombre de molécules sont aujourd’hui connues, aussi
bien au niveau de la matrice extracellulaire qu’au niveau des membranes. Nous pouvons de plus, à ce
jour, mettre en culture des cellules, et ainsi mieux comprendre les mécanismes biologiques et
cellulaires. Pour notre TP, nous voulons mettre 2 types de cellules en culture, des cellules cérébrales
et des fibroblastes. Pour les mettre en culture, nous utilisons la technique de culture de cellules
adhérentes à un support. Nos observations se font au microscope inversé, sous hotte à flux
laminaire, et donc en conditions stériles.
II. 1ère partie : mécanisme d’adhésion et de migration cellulaire
A. L’embryon et les annexes embryonnaires
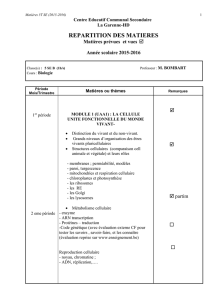
Vésicule Vitelline
Vitellus
Allantoïde
Chorion
Cœlome extra-embryonnaire
Embryon
Cavité amniotique
Amnios
Figure 1 : Schéma de l'embryon de poulet à 7 jours
de développement

Guillou Noëlline TP de culture cellulaire Chateigner Aurélien
2
Coquille
Embryon
Annexes embryonnaires
Vitellus
Allantoïde
Embryon
Amnios
Veine vitelline
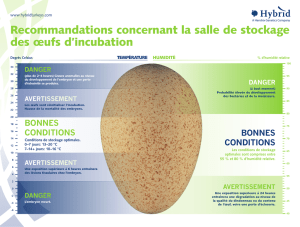
Figure 3 : Photo de la position de l'œuf par rapport aux annexes
embryonnaires une fois l’embryon extrait de l’œuf.
Figure 2 : Position relative de l'Embryon dans l'œuf, en vue du dessus, en
ayant coupé du côté du "gros bout"

Guillou Noëlline TP de culture cellulaire Chateigner Aurélien
3
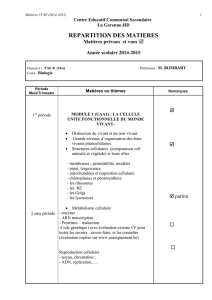
Bec
Œil
Hémisphères cérébraux
Lobes optiques
Tête
Cervelet
Moelle épinière
B. Rôle des annexes
a) Vitellus
Réserves nutritives de l’embryon, rôle nourricier.
b) Vésicule vitelline
Entoure la masse de Vitellus, sert d’organe digestif. Elle est parsemée de vaisseaux sanguins, ainsi les
produits sont absorbés par ceux-ci et transportés vers l’embryon.
c) Allantoïde :
Fonction dans la respiration : la splanchnopleure amène une vascularisation ce qui permet des
échanges gazeux entre l’allanto-chorion et la coquille de l’œuf.
Fonction nutritive sur plusieurs aspects : prend le relais du raphé séro-amniotique pour l’assimilation
du reste de l’albumen et permet de récupérer le calcium de la coquille pour former les os de
l’embryon ce qui fragilise la coquille et ainsi facilite la sortie du poussin.
Fonction excrétrice : la cavité allantoïde est une poubelle de l’embryon, en effet les déchets produits
par les reins seront lâchés dans l’allantoïde. Au moment de l’éclosion l’allanto-chorion reste collée à
la coquille.
d) Chorion
Couche extra-embryonnaire externe constituée de mésoderme et d’ectoderme.
e) Cœlome extra-embryonnaire
Cavité générale de l’œuf.
Figure 4 : Zone cérébrale d'un embryon d'œuf de poule

Guillou Noëlline TP de culture cellulaire Chateigner Aurélien
4
f) Amnios
Permet le développement de l’embryon en milieu liquide. Permet l’assimilation de l’albumen par le
raphé séro-amniotique jusqu'à 16 jours d’incubation. Assure à l’embryon une protection contre une
possible dessiccation et d’éventuels chocs mécaniques.
C. Mise en culture des cellules cérébrales embryonnaires de
poulet
Matériel et méthodes :
1. Milieu DMEM
a) DMEM base
Le milieu DMEM base est acheté tel quel.
b) DMEM 5%
Le milieu DMEM 20% se prépare en suivant la composition suivante :
- Milieu de base : DMEM 500 mL
- Sérum de veau fœtal (SVF) 25 mL (5%)
- Antibiotique 6 mL
- L-glutamine 6 mL
c) DMEM 20%
Le milieu DMEM 5% se prépare en suivant la composition suivante :
- Milieu de base : DMEM 500 mL
- Sérum de beau fœtal (SVF) 110 mL (20%)
- Antibiotique 6 mL
- L-glutamine 6 mL
2. Poly Lysine
Pour 10 boites :
1- Peser l’acide borique dans un bécher de 50 mL et ajouter 40 mL environ d’H2O
2- Ensuite, peser la poly lysine dans un micro bécher à l’aide de 2 pinces et l’ajouter avec
attention à l’acide borique. Agiter le tout.
3- Peser le NaOH 1N dans un bécher de 25 mL et ajouter de l’H2O puis mélanger avec une tige
de verre dans un bain-marie. Ensuite, le transvaser dans une fiole et ajuster à 50 mL. Agiter
et mettre dans un flacon.
4- Le PH étant de 4,75 environ, il faut (0,5 mL environ d’NaOH 1N) pour remonter le pH à 8,4
5- Ensuite ajuster la solution à 50 mL avec H2O
6- Prévoir un bécher de 25 ou 50 mL et une seringue de 10 mL avec un filtre de 0,22 µm et
verser 2,5 mL par boite de Pétri (sous la hotte). Ne plus bouger les boites jusqu’à la mise en
culture.
3. Tampon borate
Pour les boites « borate », la procédure est la même sauf que l’on n’ajoute pas la poly lysine au
tampon borate.

Guillou Noëlline TP de culture cellulaire Chateigner Aurélien
5
4. Fibronectine
On veut préparer 10 boites de 60 mm de diamètre, ayant donc chacune 28 cm² de surface. On veut 2
µg.cm-2, on a donc besoin de 560 µg de fibronectine.
Pour cela on suit le protocole suivant :
1- Reconstituer avec 1 mL d’eau stérile par mg de protéine. Laisser dissoudre pendant au moins
30 minutes.
2- Diluer la fibronectine dans une solution saline tamponnée (la dilution n’est pas indiquée) et
recouvrir la surface de culture avec un volume minimum.
3- Laisser sécher à l’air pendant au moins 45 minutes à température ambiante. L’excès de
fibronectine sera éliminé par aspiration.
Lors de notre manipulation, nous avons donc mis en culture des cellules cérébrales embryonnaires
de poulet dans des boites de Pétri présentant différents revêtements afin de savoir lequel semblait
être le plus adapté à ce type de culture cellulaire.
Protocole :
Incision
Œuf de poule à stériliser à l’alcool
Prélèvement de
l’embryon
Prélèvement des
hémisphères
cérébraux
Dans du DMEM 20%
Préparation de la culture
des fibroblastes
Homogénéiser à l’aide d’une
seringue et d’un trocart
Répartir 1,5 mL de la solution
cellulaire + 3,5 mL de DMEM
20% dans chaque boite
Fibronectine
Tampon Borate
Polylysine
Préparer les revêtements des
différentes boites
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%