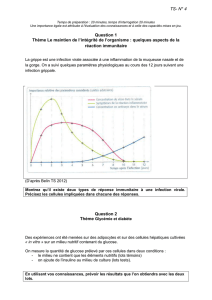
Prédiction du niveau de glucose en utilisant des réseaux

PREDICTION DU NIVEL DE GLUCOSE EN UTILISANT
DES RESEAUX DE NEURONNES
E. IANCU1, I.IANCU2, D.ISTRATE3, M. MOTA4
(1)Département Automatique/Université de Craiova, 107 Rue Decebal, 200440 Craiova, Roumanie
(2)Département de physiologie, informatique médical et bio-statistiques/Université de Médecine et
Pharmacie de Craiova, 4, Rue Petru Rares, 200349 Craiova, Roumanie
(3)LRIT /ESIGETEL, 1, Rue du Port de Valvins, 77210 Avon, France
(2)Département de diabète et maladies de nutrition/Université de Médecine et Pharmacie de Craiova, 4, Rue
Petru Rares, 200349 Craiova, Roumanie
Mots clés: niveau de glucose, contrôle automatique, réseau de neurones
1. Introduction
Le but de ces travaux de recherche est de réaliser la
prédiction du niveau de glucose dans le sang pour un
système de contrôle automatique.
Les méthodes actuelles de traitement du diabète
dépendant de l’insuline consistent dans une injection
sous-cutanée d’insuline ou dans une injection
continue d’insuline à travers une pompe. Dans ce
type de traitement le patient doit s’injecter l’insuline 5
fois par jour et la quantité est déterminée par une
mesure du niveau de glucose complétée par une
approximation du contenu de glucose du repas [1-2].
La pompe d’insuline par rapport à l’injection permet
un débit constant et prédictible.
Le control prédictive est différent du contrôle en
boucle fermé où la différence entre le point
d’opération désiré est comparée avec la concentration
actuelle de glucose et envoyée comme contre-réaction
au système. Les problèmes du contrôle prédictif sont
définis dans le domaine temporel et leurs solutions
nécessitent l’analyse de l’évolution future pour
optimiser les performances [3-4]. Utilisant la théorie
du control prédictif les déviations du niveau de
glucose dans le sang par rapport au niveau normal
peuvent être minimisées sans utiliser des grandes
quantités d’insuline en mode préventif.
L’efficacité du système de control prédictif est
mesurée comme étant la capacité à garder le niveau
de glucose dans le sang le plus proche possible du
niveau normal. Cela est essentiel pour prévenir des
complications du diabète. Idéalement, ce niveau doit
se situer entre 60 et 120 mg/dl avant les repas et plus
petit que 180 mg/dl deux heures après le début du
repas.
2. Le contrôle du niveau de glucose dans
le sang
Par rapport à la technique classique du contrôle du
glucose par injection d’insuline si le niveau du
glucose est surveillé et l’insuline est délivrée suivant
une loi proche de celle de l’organisme. Dans un
organisme en bonne santé, les cellules B délivrent
l’insuline dans le sang à deux débits :
Un débit basal continu et basal qui contrôle
la génération de glucose par le foie ;
Des quantités plus importantes mais de
courtes durées d’insuline pendant les repas
pour l’absorption intestinale du glucose.
La thérapie avec une pompe d’insuline est
recommandée comme étant la méthode la plus
efficace et physiologique dans le cas des diabètes
sucrée de type I (dépendant d’insuline). Il y a des
auteurs qui considèrent que le système à boucle
fermée (pancréas artificiel) représente une solution
très efficace [5]. Cette solution utilise un capteur de
glucose extracorporelle qui est couplé au contrôleur
programmable (PLC) qui calcule et commande le
débit de l’infusion d’insuline sous cutané pour
maintenir un niveau normal de glycémie. Ce type de
système est très efficace dans le maintien de la
glycémie dans les limites normales pour quelques
jours mais a des désavantages majeurs dans
l’utilisation à long terme. Des infusions prolongées
augmentent le risque de thrombose et infection.
Dans cette étude, le capteur extracorporelle de
glucose est couplé à une unité logique qui est
composée d’un réseau de neurones et d’un module de
prise de décisions (Figure 1). Le réseau de neurones
prédit la nouvelle valeur de glycémie en se basant sur
les valeurs précédentes. Le module de prise de

décision inclut un modèle mathématique du patient.
Ce module reçoit autant la valeur actuelle du niveau
de glucose que la valeur prédite comme valeur future
par le réseau de neurones. En se basant sur le modèle
du patient une estimation de la quantité d’insuline
nécessaire est réalisée et le débit d’insuline de la
pompe est commandé en conséquence.
Figure 1: La structure du système prédictif pour le
control du niveau d’insuline
3. L’architecture du réseau de neurones
Le réseau de neurones non récurrent, du point de vue
système, représente une cartographie statique entre
les entrées et les sorties [6]. Le réseau de neurones
utilisé est non récurrent à deux niveaux et il reçoit en
entrée les 5 dernières valeurs du niveau de glucose et
prédit la 6ème.
4. Résultats
Dans cette étude nous avons utilisé les données de 22
sujets adultes (12 femmes et 10 hommes) avec
diabète dépendant d’insuline et 8 personnes en bonne
santé. Parmi les 22, 16 patients ont suivi un traitement
à injection d’insuline et 6 avec une pompe.
L’évolution du niveau de glucose a été enregistrée
pour chaque patient, chaque 5 minutes pendant 3
jours. Chaque patient a eu une vie normale avec repas
et activités autant à la maison qu’au bureau.
Trois cas ont été pris en compte : un patient avec un
traitement classique à base d’injection (P1), un patient
avec un traitement basé sur la pompe à insuline (P2)
et une personne en bonne santé (P3).
Pour P1, une grande variabilité du niveau de glucose
a été mesurée, pour P2 la variabilité est plus réduite
mais encore importante par rapport à la personne en
bonne santé.
L’apprentissage du réseau de neurones a été effectué
pour chaque patient sur une période de 24h et le test a
été effectué sur une autre période de 24h. L’erreur de
prédiction sur les 3 patients a été plus faible que 10
mg/dl.
5. Conclusion
Un réseau de neurone non-linéaire autorégressif avec
2 niveaux a été utilisé pour prédire l’évolution du
niveau de glucose dans le sang. Le premier niveau
contient 10 neurones et utilise une fonction de
transfert de type tansig. Le 2ème niveau contient un
seul neurone et a une fonction de transfert de type
pureline.
Le système proposé utilise 5 mesures consécutives du
niveau de glucose dans le sang qui représente 25
minutes d’historique pour prédire la valeur future.
Cela donne une avance de 5 minutes dans la
commande de la pompe à insuline. L’erreur de
prédiction est faible ce qui nous encourage à
continuer nos recherches sur cette voie.
References
[1] Anne Peters Harmel, Ruchi Mathur, Diabetes
Mellitus. Diagnosis and Treatment, Saunders –
Elsevier Science, 5th edition, Philadelphia, USA,
2004, pp. 109 – 145.
[2] Ernest Mazzaferri and collaborators, Year Book of
Endocrinology 2007, Elsevier – Mosby,
Philadelphia, USA, 2007, pp. 11-30.
[3] Zarita Zainuddin, Ong Pauline and Cernal Ardil,
A Neural Network Approach in Predicting the
Blood Glucose Level for Diabetic Patients
International Journal of Computational
Intellingence, 5:1, 2009, pp. 72-79.
[4] Scott M. Pappada, Brent D. Cameron, Paul M.
Rosnan, Development of a Neural Network for
Prediction of Glucose Concentration in Type 1
Diabetes Patients, Journal of Diabetes Science and
Technology, Vol. 2, N°. 5, September 2008,
pp.792-793.
[5] B. Wayne Bequette, A critical Assessment and
Challengeles in the Development of a Closed-
Loop Artificial Pancreas, Diabetes Technology &
Therapeutics, Vol. 7, N°. 1, 2005, pp. 28-47.
[6] Raed Abu Zitar, Abdulkareem Al-Jabali, Towards
Neural Network Model for Insulin/Glucose in
Diabetics-II, Informatica 29, 2005, pp. 227-232.
Remerciements
Ces travaux font partie du projet « The development
of automated systems for blood-glucose control at
insulin-dependent patients. The implementation of
evolved algorithms for computer assisted monitoring
and diagnosis » de l’Université de Médecine et
Pharmacie de Craiova, soutenu par le Conseil
National de Recherche Universitaire.
1
/
2
100%