Fonctions des protéines de la membrane plasmique
Pascale PERRIN Plan 1/6
Plan – « Les fonctions des protéines de la membrane plasmique»
Introduction
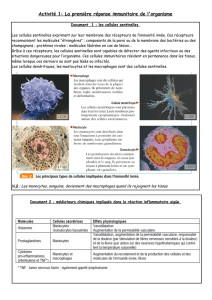
Définition de la membrane plasmique : La membrane plasmique est la membrane qui délimite une
cellule et sépare donc le cytoplasme du milieu extérieur. Elle est constituée de lipides
(phospholipides, molécules de cholestérol) et de protéines (intra-, trans- et extra-cellulaires)(et non
les organites) et d’un faible pourcentage de glucides.
Définition des protéines : une protéine est une macromolécule biologique composée par une ou
plusieurs chaîne(s) d'acides aminés liés entre eux par des liaisons peptidiques. Ces protéines
peuvent constituer près de 46% de la composition de la structure de la membrane plasmique.
La membrane plasmique joue un double rôle de protection et de régulation des échanges entre le
milieu extérieur et intérieur. Cette part protéique est variable mais elle est essentielle car elle
détermine la perméabilité ainsi que l’identité des cellules et les capacités d’adhérence. Ces
protéines ont différents modes d’interaction avec la membrane plasmique : ancrage lipidique,
transmembranaire ou périphérique (protéines intrinsèques, transmembranaires ou extrinsèques).
Trois rôles majeurs seront évoqués :
- Activités réceptrices et enzymatiques
- Echanges entre milieu extérieur et intérieur
- Rôle dans l’adhérence et la reconnaissance
I-Echanges entre milieux intracellulaire et extracellulaire – Rôle
de transport
I-1 Transports membranaires des petites molécules :
Les aquaporines sont des protéines membranaires qui assurent le passage des
molécules d’eau de part et d’autre de la membrane.
I-1-1 Canaux ioniques: toujours ouverts ou à ouverture provisoire réglée par un ligand Ö
diffusion simple des ions (équilibre de Nernst). Transport passif, dans le sens du gradient
I-1-2 Protéines transporteurs : elles ont un site de fixation et elles vont assurer la
modification de la protéine pour son intégration dans le cytoplasme. Elles permettent une diffusion
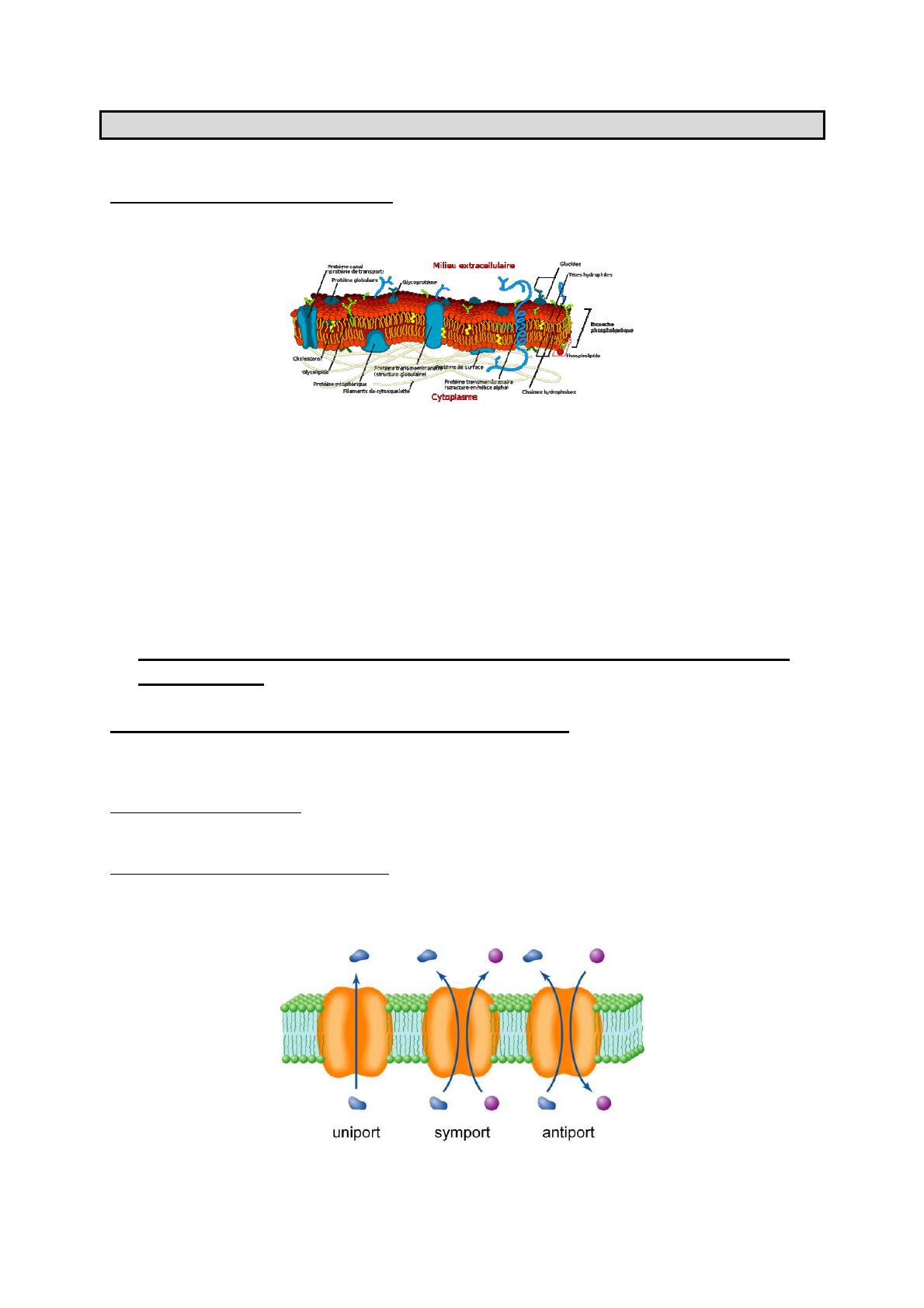
facilitée par affinité. Une protéine de transport qui laisse passer une molécule est appelée uniport.
Lorsqu’elle laisse passer deux molécules dans le même sens, elle est dénommée cotransporteur
symport, en sens inverse, elle est dénommée cotransporteur antiport.
Les molécules non chargées électriquement vont du milieu le plus concentré au moins concentré et
elles suivent leur gradient.

Pascale PERRIN Plan 2/6
Si la cellule a besoin d’absorber ou de rejeter une molécule contre son gradient, il y a couplage à
une réaction enzymatique exergonique (ATP par exemple). Il s’agit, alors, d’un transport actif.
I-2 Transports membranaires des macromolécules :
I-2-1 Endocytose : pour les macromolécules solubles, il s’agit de pinocytose. Toutes les cellules sont
capables de ce type d’endocytose. Pour les macromolécules non solubles, il s’agit de la phagocytose
et seules certaines cellules animales sont capables de phagocytose. On distingue deux types
d’endocytose selon l’aspect des puits et des vésicules :
¾ Non spécifique (sans récepteurs): lisses
¾ Spécifique : hérissées, tapissées, recouvertes (avec récepteurs)(clathrine, COP I, COP II,
dynamine), opsonine (phagocytose), cavéole, SNARE, Rab…
I-2 -2 Exocytose : pour les cellules sécrétrices
II- Activités réceptrices et enzymatiques – Transmission de signaux
Un récepteur est une structure moléculaire de nature polypeptidique qui interagit spécifiquement
avec un messager, hormone, médiateur, cytokine, ou à un contact intercellulaire spécifique. Cette
interaction crée une modification du récepteur qui conduit, par exemple, à l'ouverture du canal lié
au récepteur, ou se transmet par l'intermédiaire de réactions enzymatiques à l'effecteur distant du
récepteur. La même cellule comporte en général plusieurs types de récepteurs différents. Un
récepteur membranaire comporte une partie extracellulaire où se trouve le site de reconnaissance
de la molécule informative, une partie transmembranaire et une partie intracellulaire.
II.1 Récepteurs canaux
Ces récepteurs comportent un canal qui fait communiquer le cytoplasme avec le milieu
extracellulaire. La molécule informative module l'ouverture du canal et régule, en général, l'entrée
dans la cellule soit des cations Na+ ou Ca2+, soit d'anions Cl-.
Leur activation se traduit par un flux ionique. De nombreux neurotransmetteurs "classiques" se lient
à ce type de structure : l'acide γ-aminobutyrique aux récepteurs GABA-A, les acides aminés exci-
tateurs (glutamate, aspartate...) aux récepteurs ionotropiques NMDA et kaïnates, l'acétylcholine
aux récepteurs nicotiniques, l'ATP aux récepteurs P2x.
Ces récepteurs-canaux sont à différencier, d'une part des canaux voltage-dépendants dont
l'ouverture est régulée par le potentiel membranaire, une dépolarisation cellulaire favorisant leur
ouverture, et d'autre part des canaux dont l'ouverture est régulée par l'intermédiaire d'une variation
de la concentration intracellulaire du Ca2+, de l'AMPc ou du GMPc.
¾ Les récepteurs-canaux cationiques :
• Récepteurs nicotiniques avec canal ionique (sodique) présents au niveau du système nerveux
et des muscles squelettiques
• Récepteurs HT3 de la sérotonine
• Récepteurs du glutamate et de l'aspartate
L'ouverture des canaux cationiques, en favorisant l'entrée de Na+ et ou du Ca2+ dans la cellule,
entraîne une dépolarisation et une augmentation de l'excitabilité.
¾ Les récepteurs-canaux anioniques comme le canal chlorure Cl-:
• Récepteurs GABAA, auxquels sont associés les récepteurs aux benzodiazépines qui modulent
l'ouverture du canal perméable aux ions Cl-
• Récepteurs de la glycine qui favorisent aussi l'ouverture des canaux Cl-.
La pénétration des ions Cl- dans la cellule augmente sa polarisation et diminue son excitabilité.

Pascale PERRIN Plan 3/6
II.2 Récepteurs enzymes
Le récepteur possède lui-même une activité enzymatique. Son activation par le messager module
cette activité qui est de type kinase ou phosphatase ou guanylate cyclase :
¾ de type protéine kinase. La plupart d'entre eux sont des récepteurs tyrosine kinases,
désignés habituellement par RTK, un des plus connus étant le récepteur à l'insuline
(schéma ci-dessus), mais il en existe aussi à activité sérine/thréonine kinase. Le
récepteur de l'insuline est formé de deux sous-unités a et de deux sous-unités ß.
¾ de type guanylate cyclase. L'activation de ce récepteur-enzyme provoque la
formation, à partir de la guanosine triphosphate (GTP), de guanosine
monophosphate cyclique (GMPc) qui active des protéines kinases.
II-3 Récepteurs liés aux protéines G
Les récepteurs liés aux protéines G sont ainsi appelés parce que leur activité nécessite la présence
de guanosine diphosphate (GDP) qui est phosphorylée pour donner la guanosine triphosphate (GTP).
Cette phosphorylation pourrait être couplée à un transfert préalable de protons comme source
d'énergie.
Les récepteurs liés aux protéines G sont de nature polypeptidique et comportent une partie
extracellulaire portant le site de liaison avec le messager, une partie transmembranaire à sept
hélices (parce que la chaîne polypeptidique traverse la membrane sept fois) et une partie
intracellulaire en contact avec les protéines G qui assurent le transfert et l'amplification du signal
reçu par le récepteur.
Chaque protéine G est hétérotrimérique, c'est-à-dire constituée de trois sous-unités différentes a, ß
et g, ces deux dernières formant un complexe hétérodimérique. La stimulation du récepteur conduit
à leur dissociation.
La grande majorité des neuropeptides se lie à cette dernière famille de récepteurs.

Pascale PERRIN Plan 4/6
III- Rôle dans l’adhérence et la reconnaissance
III-1 Adhérence cellule/cellule
III-1-1 rôle des molécules d’adhérence dans l’assemblage cellulaire
Jouent un rôle important dans le développement et l’intégrité anatomique des tissus :
- N-CAM
- Dans la compaction embryonnaire : cadhérines liées soit à des β-caténines soit à des α-
actinine, elles-mêmes liées au cytosquelette.
III-1-2 Rôle des molécules d’adhérence dans les la circulation de cellules immunitaires
L’inflammation attire les cellules immunitaires compétentes.
Dans leur état normal, il existe une liaison faibles entre les leucocytes et les cellules endothéliales
(par le biais de sélectines E- et P-).

Pascale PERRIN Plan 5/6
En cas d’inflammation, il y a relarguage de chémokine par les cellules endothéliales voisines de
l’inflammation. Cela favorise la traversée des leucocytes entre les cellules endothéliales en activant
les intégrines à la surface des leucocytes.
III-1-3 Molécules d’adhérence dans la cohésion cellulaire
Il existe trois types communs de jonctions dans les cellules animales : jonctions serrées ou
étanches, jonctions d’ancrage ou adhésive et jonctions gap ou communicantes.
¾ jonctions serrées ou zonula occludens : ces jonctions ne sont pas totalement étanches mais elles
nécessitent des transporteurs membranaires sélectifs. Plusieurs molécules d’adhérence sont
impliquées :
- occludine
- claudine
- JAM (junctional adhesion molecule)
Elles constituent un réseau de fibrilles. Ces jonctions serrées sont liées à des protéines
intracellulaires de type ZO-1 et ZO-2 qui se lient au cytosquelette (actine) dans le domaine apical
de la cellule.
¾ jonctions d’ancrage ou zonula adherens et desmosomes qui assurent l’attachement mécanique
des cellules entre elles.
Pour la zonula adherens, les liaisons se font avec les filaments d’actine alors que pour les
desmosomes, les liaisons se font avec les filaments intermédiaires comme la kératine. Les deux font
intervenir des molécules transmembranaires d’adhérence telles que les cadhérines.
Pour la zonula adherens, il y a liaison de la E-cadhérine à la β-caténine, elle-même liée à l’actine.
Pour le desmosome, il y a liaison de la cadhérine sous forme de desmogléine et de desmocolline liée
à la desmoplakine qui fixe les filaments intermédiaires.
III-2 Adhérence cellule-matrice extra-cellulaire (MEC)
La fibronectine organise la matrice et favorise l’adhérence des cellules à la MEC. Cela se fait en
particulier par le motif RGD (arg-Gly-Asp) qui assure la fixation des intégrines. Idem pour les
laminines.
A l’intérieur de la cellule, les intégrines interagissent avec le cytosquelette ? Pour leur interaction
avec la MEC, elles sont assemblées en amas, les points focaux d’adhérence.
 6
6
1
/
6
100%