Chapitre V : Les médicaments du système reproducteur Hormones

Chapitre V : Les médicaments du système reproducteur
Hormones de l’hypophyse antérieure (rappel) : cfr chapitre II page 6
Structure et synthèse des stéroïdes sexuels naturels
Stéroïdes sexuels naturels : relation structure-activité
L’axe hypothalamo-hypophyso-testiculaire
Effets des androgènes sur le développement embryonnaire
Mécanismes d’action et effets des androgènes
Dérivés semi-synthétiques des androgènes
Utilisation thérapeutique des androgènes et anabolisants
Médicaments de l’impuissance
Anti-androgènes
Inhibiteurs de la 5α-réductase
L’axe hypothalamo-hypophyso-ovarien
Cycle ovarien et utérin
Mécanisme d’action des estrogènes (1)
Mécanisme d’action des estrogènes (2)
Estrogènes naturels et synthétiques
Effets des estrogènes (1)
Effets des estrogènes (2)
Modulateurs sélectifs des récepteurs aux estrogènes (SERM)
SERM et inhibiteurs de l’aromatase
Progestatifs naturels et synthétiques
Progestérone
Gonadoréline et analogues
Gonadotrop(h)ines
Utilisation thérapeutique des associations estroprogestatives
Utilisation thérapeutique des associations estroprogestatives
Contraception hormonale (1)
Contraception hormonale (2)

GHRH
(somatoréline)
CRH
(corticolibérine) GnRH
(gonadoréline) Dopamine
TRH
(protiréline)
Somatostatine
inhibition
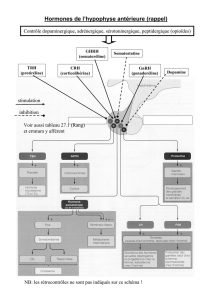
Hormones de l’hypophyse antérieure (rappel)
stimulation
Contrôle dopaminergique, adrénergique, sérotoninergique, peptidergique (opioïdes)
NB: les rétrocontrôles ne sont pas indiqués sur ce schéma !
Voir aussi tableau 27.1 (Rang)
et erratum y afférent

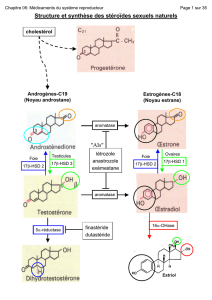
Structure et synthèse des stéroïdes sexuels naturels
aromatase
aromatase
Androgènes-C19
(Noyau androstane) Oestrogènes-C18
(Noyau estrane)
cholestérol
5α-réductase
NB: 17β-HSD type 1 : ovaires
17β-HSD type 2 : foie
17β-HSD 1
17β-HSD 2
Phyto-oestrogènes
(isoflavones)
17β-HSD 1
17β-HSD 2
16α-OHase
Oestriol

OH
(not for progesterone)
(not for progesterone)
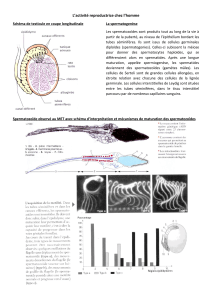
Stéroïdes sexuels naturels : relation structure-activité

Production de testostérone par les cellules de Leydig = ~4-10 mg/jour
Concentration plasmatique ~ 5 ng/mL; liaison à la SHBG (65%) et à l’albumine (33%)
Transformation en oestradiol => rétrocontrôle SNC, minéralisation osseuse, spermatogenèse
DHT => effets périphériques
Dégradation hépatique en androstènedione => T1/2 ~20 minutes => testostérone inactive p.o.
FSH et testostérone sont toutes deux indispensables à la spermatogenèse
L’axe hypothalamo-hypophyso-testiculaire
GnRH = décapeptide
= LH
INHIBINE
Rang
Fig 29.4
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
1
/
29
100%