Régulation physiologique de l`axe gonadotrope chez la femme

Du sexe génétique au sexe phénotypique :
Nous avons déjà travaillé sur la reproduction sexuée en étudiant la méiose et la fécondation.
Cette reproduction apparait dès les Eucaryotes unicellulaires. Dans le groupe des vertébrés, chez les
mammifères placentaires, elle se caractérise par l’acquisition de la viviparité. Cependant la
fécondation d’un ovocyte par un spermatozoïde donne une cellule œuf. Cette dernière est à l’origine
au cours du développement embryonnaire de tissus biens différenciés, et en particulier de tissus et
de migrations cellulaires qui élaborent l’appareil uro-génital.
Sachant que le sexe génétique d’un organisme est déterminé par ses chromosomes sexuels.
Nous allons essayer de comprendre chez les mammifères placentaires comment un appareil génital
mâle apparait chez un individu XY et une femelle pour un individu XX. En fait nous étudierons très
simplement les mécanismes responsables du phénotype sexuel à partir du génotype.
Chez les mammifères la structure et la fonctionnalité des appareils sexuels mâles et femelles
sont acquises en 4 étapes au cours du développement :
1er stade phénotypiquement indifférencié : chez un individu génétiquement déterminé se mettent en
place des gonades phénotypiquement indifférenciées et deux types de voies génitales : les canaux de
Wolf et de Muller.
2ème stade : du sexe génétique au sexe gonadique : nous venons de dire que normalement
génétiquement déterminé un mâle est XY et une femelle XX, pourtant il a été mis en évidence des
caryotypes masculins 46XX et des féminins 46XY : ces anomalies peuvent être interprétées par la
translocation d’un court fragment de la région distale du bras court du chromosome Y sur X lors de al
gamétogénèse. En effet sur la partie spécifique de ce chromosome se trouve le gène SRY responsable
du phénotype mâle.
L’expression de ce gène dans les gonades permet la formation d’une protéine TDH (facteur de dev
testiculaire, qui possède un domaine de liaison avec l’ADH). Ce facteur va activer de nombreux gènes
conduisant à la différenciation des gonades en testicules ce qui va provoquer l’acquisition du sexe
gonadique mâle.
3ème stade : du sexe gonadique au sexe phénotypique : Des observation à partir d’animaux « free-
martin » et des expériences ont permis de mettre en évidence une production de testostérone
parles cellules interstitielles et d’hormone antimüllérienne AMH par les cellules de Sertal. Ce sont
ces deux hormones qui contrôlent la masculinisation de l’appareil génital. On observe alors une
involution des canaux de Muller et une différenciation de ceux de Wolf e, épididyme, canal
déférent, et vésicule séminale. A l’inverse les ovaires n’ont pas de rôle dans le développement de
l’appareil génital féminin. C’est en effet l’absence d’hormone testiculaire qui permet l’involution des
canaux de Wolf et la persistance et différenciation de ceux de Muller en oviductes et corne utérines.
Les hormones ovariennes sont par contre responsables de l’acquisition de la fonctionnalité de
l’appareil génital féminin.

TP14
4ème étape : la puberté : le commencement de la puberté chez la femme est plus précoce que chez
l’homme. Elle correspond à l’acquisition de la fonctionnalité des appareils sexuels ainsi qu’à des
changements morphologiques et comportementaux chez l’adolescent ; Ces transformations mettent
en place les caractères sexuels secondaires comme la pilosité faciale et corporelle, la masse
musculaire, la localisation des masses graisseuses, la voix…
L’ensemble de ces processus sont sous la dépendance et le contrôle des hormones sexuelles. C’est
l’augmentation de la sécrétion de ces hormones qui induit le début de la puberté et permet le
maintient de ces caractéristiques.

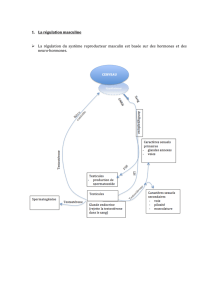
Régulation physiologique de l’axe gonadotrope chez l’homme
A partir de la puberté les testicules produisent des spermatozoïdes et de la testostérone de manière
continue jusqu’à la fin de la vie. Cependant si on analyse la sécrétion journalière ou horaire de
l’hormone on observe une sécrétion pulsatile qui reste autour d’une valeur moyenne. Cet aspect
pulsatile met en évidence une régulation de la sécrétion de testostérone. Nous allons dans ce
chapitre nous intéresser à cette régulation indispensable à la fonctionnalité de l’appareil génital
mâle. Nous terminerons en établissant un schéma fonctionnel de ce système de régulation.
Le testicule origine de la production de spermatozoïdes (TP15):
*on peut distinguer des tubes séminifères qui contiennent des cellules souches des cellules
germinales (spermatogonies) mais également les cellules germinales (spermatocytes I et II : bord du
tube) qui après une première divisions méiotique deviennent des spermatides puis en fin de méiose
des spermatozoïdes (lumière du tube). L’ensemble de ces cellules est soutenu par des glandes
cellulaires : les cellules de Sertoli qui assurent aussi la nutrition. (Contrairement aux ovocytes les
spermatozoïdes sont mobiles).
Les spermatozoïdes comprennent une tête contenant ne
noyau, une partie intermédiaire où est fabriquée l’énergie
nécessaire au mouvement et d’un flagelle origine du
déplacement.
*Les cellules interstitielles que l’on observe entre les tubes sont le lieu de production de
testostérone, le testicule peut donc également être considéré comme une glande endocrine
(fabrique et sécrète une hormone). La testostérone est en suite véhiculée par le sang et agit sur les
cellules cibles qui disposent des récepteurs spécifiques (+ ou – éloignées).
Les activités testiculaires sont régulées par le complexe hypothalamo-hypophysaire :
L’hypophyse est une glande comprenant chez les mammifères 2 parties différentes (déjà au niveau
embryonnaire) : * l’hypophyse antérieure ou adéno-hypophyse constituée de cellules endocrines
responsables de la production continue d’hormones LH et FSH (hormones lutéales et de stimulation
folliculaire) qui sont des gonadostimulines.
*l’hypophyse postérieure ou neuro-hypophyse constituée de terminaisons
nerveuses, de neurones dont les corps cellulaires se situent dans les noyaux hypothalamiques.

La sécrétion de testostérone ainsi que la
production de spermatozoïdes sont régulés par
la production continue de gonadostimuline.
Cependant la sécrétion pulsatile de LH et de FSH
est sous la dépendance d’informations de
l’hypothalamus.
Liaison hypothalamo-hypophysaire le système
porte : les noyaux hypothalamiques contiennent
des neurones dont certains libèrent au niveau
de la tige épituitaire de la GnRH est une neuro-
hormone (molécule synthétisée et sécrétée dans
le sang par un neurone, le sans la véhicule ensuite jusqu’aux cellules cibles qui possèdent les
récepteurs spécifiques).
La GnRH agit sur des récepteurs membranaires des cellules à FSH et LH, des expériences montrent
des bouffées de potentiel d’action présents sur les axones des neurones sécréteurs sont à l’origine
du caractère pulsatile des sécrétions (sur tout le processus).
La testostérone est responsable d’un rétrocontrôle négatif : des observations montrent que la
sécrétion de GnRh ainsi que celle de FS et de LH sont régulées et modifiées par la taux plasmatique
de testostérone ou testostéronémie. On constate également à partir d’expériences de marquage
radioactif qu’il existe des récepteurs à la testostérone au niveau des cellules hypothalamiques
sécrétrice de GnRH ainsi que des cellules sécrétrices de LH et de FSH.
La sécrétion de testostérone par les cellules de Leydig soumises à l’action de LH va rétroagir sur
l’hypophyse et sur l’hypothalamus. Ce mécanisme physiologique qui provient de la variation du taux
de testostérone et qui s’oppose à cette variation s’appelle rétrocontrôle négatif. Ainsi la
testostéronémie oscille en permanence autour d’une valeur moyenne.
Action des centres nerveux supérieurs : les neurones hypothalamiques possèdent d’innombrables
connexions avec des régions du système nerveux central. Les messages nerveux afférents par
l’hypothalamus vont alors modifier son activité et donc influer sur la production de GnRH (et donc de
gonadostimulines et de testostérone).
On peut alors expliquer des résultats expérimentaux comme l’évolution du volume testiculaire chez
le bélier par des modifications de facteurs de l’environnement tels que l’intensité lumineuse au cours
de l’année.
Il ne faut enfin par oublier qu’il existe des stimuli internes capables de modifier l’activité de l’axe
gonadotrope, le stress par exemple.
Les expériences réalisées ou les résultats étudiés en TP nous ont permis de construire étape par
étape et élément par élément un schéma de régulation de l’axe gonadotrope chez l’Homme :

Pour déterminer l’origine de la régulation de certaines fonctions le protocole « classique » utilisé
consiste en 4 étapes : *enlever l’organe que l’on suppose impliqué (s’il l’est la fonction n’est plus
active), *effectuer sa greffe à un endroit différent (si la fonction reprend on peut supposer une action
endocrine car la revascularisation permet de transporter une molécule chimique pas un message
nerveux), *injecter des extraits de cet organes broyé (pour confirmer qu’il est bien le sécréteur d’une
ou plusieurs hormones impliquée), *purifier la molécule active et vérifier son action par injection.
Nous ferons de même pour étudier les différents cycles régulés de l’axe gonadotrope chez la femme.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%