Transport des gaz dans le sang

Chapitre 9 :
Transport des gaz dans le sang
Docteur Sandrine LAUNOIS-ROLLINAT
Année universitaire 2011/2012
Université Joseph Fourier de Grenoble - Tous droits réservés.
UE3-2 - Physiologie – Physiologie Respiratoire

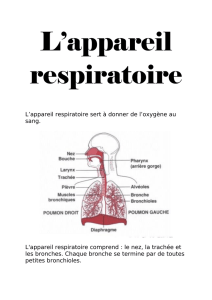
Ventilation
pulmonaire
Transport
des gaz
Echanges gazeux
Echanges gazeux
Respiration cellulaire
Transport des gaz dans le sang
Contrôle

Transport des gaz dans le sang
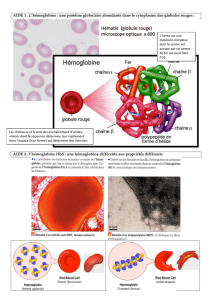
• Généralités
• Structure et propriétés de l’hémoglobine
• Transport de l’oxygène
• Transport du CO2
• Interactions

Transport des gaz dans le sang
• L’O2et le CO2sont transportés par la
circulation sanguine
– des poumons vers les tissus
– des tissus vers les poumons
• Le sang fixe l’O2et le CO2
– de manière réversible
– sous l’influence d’un gradient de pression
partielle

Transport des gaz dans le sang
•Gaztransportés en milieu liquide (plasma, cytoplasme
du GR)
• Dans un liquide, un gaz peut être présent sous 2
formes:
– dissoute
– combinée à un transporteur ou après réaction
chimique
• Seule la fraction dissoute du gaz participe à la pression
partielle
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
1
/
37
100%