T3fin 2013

T3fin 2013

T3fin 2013
Pointdefusion
Rappel:Lepointdefusionestinfluencéparlesforces
intermoléculairesquielles,sontinfluencéesparla
structuredelasubstance,ellemêmeinfluencéeparles
liaisonschimiquesquilaforme.
Expliquelatendancepériodiquedela3
e
période.
(deNaàAr)
.
T°(K)

T3fin 2013
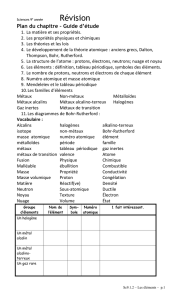
Pointsdefusiondesalcalinsetdeshalogènes
Expliquelatendancedupointdefusiondes
alcalinsetdeshalogènes.
.

T3fin 2013

T3fin 2013
Lespropriéteschimiques
Les
métauxalcalins
propriétésphysiques
:mous(peuventêtrecoupésavec
uncouteau,malléables,decouleurargentée,bons
conducteursd'électricitéavecdespointsdefusion
peu
élevés
comparésauxautresmétaux(parcequechaque
atomecontribueseulementunélectronàlaliaison
métallique)etunedensité
peuélevée
.
propriétéschimiques
:trèsréactifs
parcequ'ilsont
seulementunélectrondansleurcouchedevalencequi
esttrèsfacilement«perdu».
Formenttousdescationsayantunechargede+1et
formentdescomposésioniquesaveclesnonmétaux.
Laréactivité
augmente
endescendantlegroupe.
Rappel:Lesélémentsd'un
mêmegroupe
réagissentde
façonsemblablecarilsontlemêmenombred'électronsde
valence.
Laréactivitédesmétauxalcalins
Lesmétauxalcalinset
l’eau
(déplacementsimple)
Lesalcalinsréagissentavecl'eaudefaçonexothermiquepour
produiredel'hydrogèneetunhydroxydedemétal.Onlesappelle
desmétauxalcalinscarlasolutionrésultateestalkaline(basique)
libérantdesionshydroxydes(OH
‐
).Ilsformentdonctousdes
solutionbasique
Lithium+eau
lelithiumflottesurl'eauetréagitassezlentementengardant
saforme.
2Li+2HOH→2LiOH+H
2
sodium+eau
lesodiumréagitassezvigoureusementquelachaleurproduite
estsuffisantepourfairefondrelemétalrestantquiformentune
petiteboulequisepromènesurlasurfacedel'eau.
2Na+2HOH→2NaOH+H
2
potassium+eau
lepotassiumréagitencoreplusviolemmentetproduitassezde
chaleurpourenflammerl'hydrogèneproduitformantuneflamme
lilastoutensedéplaçantrapidementsurlasurfacedel'eau.
2K+2HOH→2KOH+H
2
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%