I. Réponse immunitaire innée anti-infectieuse

Immunologie – Hicham Bouhlal.
Cours d’Inès Masmoudi. DCEM1 2010-2011.
IMMUNITE ANTI-INFECTIEUSE & ECHAPPEMENT AU SYSTEME
IMMUNITAIRE
- La réponse immunitaire anti-infectieuse est fonction :
o Structure : LPS, nucléocapside, activation ou pas du complément.
o Reconnue ou non par des récepteurs de l’immunité innée : TLR, récepteur du
complément, etc.
o Production de substances chimiotactiques (PNN, phagocytes, etc.).
o Voie de pénétration : muqueuse/cutanée/respiratoire, etc. barrière
physique/chimique, rôle des sIgA.
o Mécanisme de pathogénécité : exemple rôle des anticorps neutralisants en cas
d’exotoxine.
o Intracellulaire ou extracellulaire : immunité cellulaire (pathogène intracellulaire)
/immunité humorale (pathogène extracellulaire).
- Rôle majeur lors des primo-infections :
o Elimination de la majorité des agents infectieux.
o Si on n’arrive pas à éliminer le pathogène, amorce de l’immunité anti-infectieuse
spécifique (rôle des cellules dendritiques). Risque d’immuno-pathologie : cette infection
peut être à l’origine d’un emballement de la réponse immunitaire avec auto-immunité.
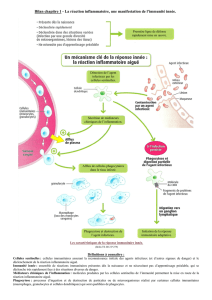
I. Réponse immunitaire innée anti-infectieuse
- Barrière physique-chimique : peau, mucus, cils, enzymes gastriques, acidité.
- Facteurs solubles : défensines et enzymes Neutralisation ou lyse de l’agent infectieux.
- PAMP-PPR.
- Déclenchement de la cascade de complément :
o Qui permet la formation du complexe d’attaque membranaire lyse du pathogène.
o Opsonisation des pathogènes par macrophage.
- Production d’IL1, TNF, IL-6 :
o Fièvre : capable de neutraliser le virus parfois rien qu’en augmentant la température.
o IFN1 : caractéristique de la réponse innée rôle antivirale, protection.
- NK.

Immunologie – Hicham Bouhlal.
Cours d’Inès Masmoudi. DCEM1 2010-2011.
1. Barrière physique-chimique
- Peau et muqueuse.
Système muco-cilaire trachéo-bronchique : de la trachée bronchioles respiratoires mucus
qui piège les particules inhalées de plus de 5μm cils carrefour oro-pharyngé où elles sont
dégluties Macrophages alvéolaires : alvéoles (<5μm).
- Acidité gastrique.
- La bile.
- Les enzymes du tractus gastro-intestinal.
2. Facteurs solubles – enzymes
- Lysozyme (épithélium, PNN monocytes) : lyse du peptidoglycane de la paroi bactérienne.
- Lactoferrine et transferrine (épithélium, PNN) : captation du fer et activité bactéricide propre.
- SLPI (épithélim) : activité modeste, Gram +, Gram-, VIH.
- Surfactant protéine A et D = SP-A et SP-D (pneumocyte II) : phagocytose activation des PNN
modulation de la production de cytokines.
- Défensines et cathélicidines (épithélium, PNN) : destruction de la membrane cytoplasmique des
bactéries, des levures, des champignons et des virus enveloppés.
- Défensines :
o Interagit avec les récepteurs à la surface des cellules avant même la pénétration des
barrières.
o Une fois le virus rentre, ces mêmes défensines peuvent diminuer l’expression de
certains récepteurs (tels que CXCR4) : permet de diminuer l’infection des cellules qui
exprime CXCR4.
o Recrutement de certaines chimiokines.
o Actions sur les PNN en produisant un peptide de neutralisation spécifique des
neutrophiles qui va agir sur le pathogène et empêcher la réplication virale dans les
cellules CD4+.
o Elles sont capables de s’intégrer dans l’enveloppe virale et perturber la relation entre
virus et cellule cible.

Immunologie – Hicham Bouhlal.
Cours d’Inès Masmoudi. DCEM1 2010-2011.
3. Récepteurs de la réponse immunitaire anti-infectieuse innée
- Reconnaitre un agent infectieux sans l’avoir jamais rencontré.
- Récepteurs PRR pour pattern recognition receptors :
o Synthétisés de manière constitutive.
o Capacité de reconnaître des «molécules signature» des agents pathogènes, PAMP pour
pathogen associated molecular patterns.
- Mannan binding protein : lectine de type C résidu mannose terminal activation de la
cascade du complément (MBL).
- Scavenger récepteur (« récepteur poubelle ») polymères anioniques LDL métabolisme des
lipides : phagocytose VCH.
- Récepteur du mannose (MR) lectine de type C -6> résidus mannose LPS, mannane gp120 VIH.
- CD14 corépceuter des TLR, phagocytose, clearance du LPS.
- TLR :
o Transmembranaire :
o Domaine extracellulaire (récepteur).
o Domaine intracellulaire qui permet d’induire un signal.
o TLR 3 : ARN double brin virus.
o TLR 9 : ADN bactérien comme dinucléotides poly-cyctéine guanine (CpG) hypo-
méthylés bactéries.
4. Fièvre
- La fièvre est la conséquence de signaux donnés à l’hypothalamus pour élever la température du
corps au dessus des valeurs normales.
- La fièvre est une des composantes de la réponse innée.
o A l’infection.
o A l’inflammation.
- Les pyrogènes exogènes : origine infectieuse.
o LPS des membranes des bactérines gramme-.
o Les peptidoglycanes des GB- et BG+.
o Les toxines sécrétées par les bactéries.
o Différents produits d’origine : virale, mycosique et parasitaire.
o PAMP PRR.

Immunologie – Hicham Bouhlal.
Cours d’Inès Masmoudi. DCEM1 2010-2011.
- Agents pyrogènes endogènes : PAMP PRR.
o LPS reconnu par CD14-TLR4/
o Activation du macrophage.
o Production de cytokines qui agissent sur l’hypothalamus.
5. Système du complément
- L’aboutissement de la cascade du complément : lyse du pathogène par le complexe d’attaque
membranaire.
- Déclencheurs :
o Résidus malin.
o Présence d’un anticorps (voie classique).
6. Phagocytose (cf. cour phagocytose)
- Capture :
o Interaction directe : TLR ? lectines (mannose, galactose), etc.).
o Interaction indirecte : opsonisation.
o Complément : CR1, CR2, CR3 (C3bi), CR4.
o Ig : FcR (IgG, FcγRI, FcγRII).
- Phagocytose.
7. Inflammation (cf. cours inflammation)
- 4 signes : chaleur, rougeur, tuméfaction et douleur.
- Cytokines pro-inflammatoire : TNF-α, IL-β, IL-6.
8. Cytokines exemple des IFN
- IFN type I : INFα et IFNβ.
o Cytokines de l’immunité innée.
o Production déclenchée par des dérivés de pathogènes :
o IFN β : au niveau des cellules épithéliales fibroblastiques.
o IFN α : au niveau des cellules dendritiques et macrophages.
- IFN type II : gamma.
o Cytokine Th1 immunité cellulaire.

Immunologie – Hicham Bouhlal.
Cours d’Inès Masmoudi. DCEM1 2010-2011.
IFN type I
- Virus ou produits viraux qui induisent la production d’IFN type I.
- IFN type I se fixe à son récepteur :
o Signalisation via JAK-STAT.
o Cela permet l’induction de l’expression des gènes cibles de l’IFN (ISGs).
o Réponse antivirale, antiproliférative et immuno-régulation de la cellule hôte.
9. Cellules NK
- Cytotoxicité : granules perforine et granzyme.
- Fas/FasL : induit apoptose et mort de la cellule.
- Sécrétion de cytokines: IFNγ +++, mais aussi TNFα, GM-CSF… :
o Stimulation macrophages et cellule dendritique.
o Augmentation présentation CMH classe II.
o Rôle dans la différenciation Th1 (IFN-γ, etc.).
10. Résumé
- Renforcement réciproque des composantes de l’immunité innée :
o L’inflammation : recrutement des phagocytes.
o L’activation du complément induit l’inflammation : chimiotactisme par C3a, C5a.
o Opsonines facilitent la capture des gants infectieux par les phagocytes.
o Le TNFα, IL-1 et l’IFN activent les phagocytes.
II. Réponse immunitaire spécifique anti-infectieuse
- Rôle majeur lors des primo-infections en cas d’échec de l’immunité non spécifique et lors des
infections secondaires (mémoire).
- Humorale :
o Neutralisation de toxines et d’enzymes bactériennes.
o Activation du complément.
o Immobilisation de l’agent infectieux.
o Inhibition de la liaison de l’agent infectieux à sont récepteur : anticorps neutralisant les
virus.
o Opsnoinsation.
o ADCC.
 6
6
 7
7
 8
8
1
/
8
100%