Embryologie 2 avril 2003

1
Embryologie 2 avril 2003.
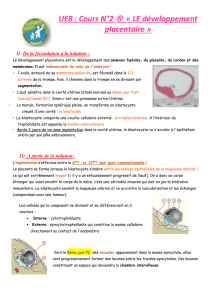
LE PLACENTA
Le placenta est un organe complexe constitué par l’association du chorion fœtal et d’une
partie d’endomètre de l’utérus.
Il a une fonction essentielle car les échanges foeto maternelles se font quasi exclusivement par
son intermédiaire.
Rappel :
A 6 jour : Le zygote est au stade de blastocyste constitué du bouton embryonnaire et d’une
couronne trophoblastique. Il s’implante sur l’épithélium endométrial utérin du côté du bouton
embryonnaire et c’est dès ce stade que le trophoblaste commence à sécréter l’HCG (hormone
coorganic gonadotrophique) qui est le premier signe biologique de grossesse.
A 7 jour : C’est le stade prélacunaire, le blastocyste est partiellement inséré dans le stroma de
la muqueuse utérine. Le trophoblaste est constitué d’une couche interne : le cytotrophoblaste
et d’une couche externe : le syntitiotrophoblaste. Ce sont les cellules cytotrophoblastique qui
prolifèrent puis migrent dans le syntitiotrophoblaste. A l’inverse dans le syntitiotrophoblaste il
n’y a pas de mitose observé mais il a une activité invasive très active du stroma utérin
oedématié, hypervascularisé et riche en glandes endométriales à mucus et en glycogène. Seul
le syntitiotrophoblaste est en contact avec le stroma utérin.
A 9 jour : On est au stade lacunaire. Avec apparition des lacunes au sein du
syntitiotrophoblaste ; l’ensemble du trophoblaste (cyto et syntitio) s’est considérablement
développé. Les capillaires maternelles sinusoïde sont congestifs, dilatés et sinusoides.
A 12/13 jour : IL y a invasion par le syntitiotrophoblaste des parois endothéliales des
capillaires sinusoïdes et c’est donc à ce stade que s’établit la première ébauche de la
circulation utéro placentaire. On constate aussi les premières proliférations (expansions)
radiaires du cytotrophoblaste à l’intérieur du syntitiotrophoblaste, ce qui constitue les
villosités primaires. Le développement de ces villosités est plus marqué au niveau du pole
embryonnaire qu’au pole anti embryonnaire. A ce stade, le mésoblaste extra embryonnaire
somatopleural tapisse la face interne du cytotrophoblaste. L’ensemble constitué par la
somatopleure extra embryonnaire et le trophoblaste qu’on dénomme le chorion.
A la fin de la 3eme semaine : les expansions cytotrophoblastiques qui commencent entre
12/13 jours atteignent la périphérie et confluent pour former la coque cytotrophoblastique
externe. Schéma : Avant que les expansions cytotrophoblastique atteignent l’endomètre utérin
c’est exclusivement le syntitiotrophoblaste qui est au contact de l’endomètre ; une fois que ces
expansions atteignent l’endomètre il y aura à la fois du syntitio et du cytotrophoblaste au
contact de l’endomètre et une fois que la coque cytotrophoblastique externe est totale, il n’y
aura plus que le cytotrophoblaste au contact de l’endomètre utérin.
Deuxième élément, à la fin de cette 3eme semaine le mésenchyme somatopleural pénètre à
l’intérieur des villosités pour former les villosités secondaires puis des vaisseaux se forment
au sein du mésenchyme villositaires pour former les villosités tertiaires. Schéma : On voit
qu’à ce stade les lacunes ne sont pas encore confluentes : ce n’est qu’au cours de la 4eme
semaine que toutes ces lacunes vont entrer en communication les unes avec les autres.
A la fin du 1er moi : Toutes ces lacunes qui ont confluées forment la chambre intervilleuse
(entre les villosités choriales) qui contient le sang maternel. Chambre intervilleuse qui est
bordé exclusivement par du syntitiotrophoblaste. Schéma : On voit que ça ne peut être que le
syntitiotrophoblaste au contact du sang maternelle qui remplit la chambre intervilleuse.

2
A aucun moment le sang maternelle n’est au contact ni ne se mêle avec le sang fœtale. Le
sang maternelle est dans la chambre intervilleuse, le sang fœtale circule dans les capillaires au
centre des villosités. Ces deux circulations sont de part et d’autre de la barrière placentaire.
Les échanges entre les deux circulations nécessaires se font par l’ensemble des mécanismes
de transport transmembranaire qu’on a vu : diffusion simple, transport actif, tout est mis à
contribution à travers les différentes structures de la barrière placentaire.
Récapitulation de ces villosités primaires, secondaires et tertiaires :
- Primaire : c’est depuis le centre vers la périphérie : l’expansion cytotrophoblastique
entouré par du syntitiotrophoblaste au contact du sang maternelle.
- Secondaire : Du centre à la périphérie : mésenchyme, couronne cytotrophoblastique,
couronne syntitiotrophoblastique.
- Tertiaire : Capillaire bordé par un endothélium, mésenchyme, cytotrophoblaste,
syntitiotrophoblaste. A ce stade, l’O2 (par exemple) doit pour atteindre le sang fœtal
franchir le syntitiotrophoblaste, le cytotrophoblaste et sa lame basale sur son versant
interne, le mésenchyme, l’endothélium avant de se retrouver dans le sang fœtal.
Dans la mesure où toutes ces villosités baignent directement dans le sang maternelle contenu
dans la chambre intervilleuse, on parle de barrière placentaire de type hémochoriale.
Ces villosités vont se développer et on va observer la prolifération de nouvelles villosités à
partir des villosités préexistantes selon le même mécanisme que celui de la formation des
toutes premières villosités. Schéma : D’abord un bourgeonnement trophoblastique, ce
bourgeonnement est envahit par l’expansion cytotrophoblastique puis est envahit
ultérieurement par le mésenchyme puis par les vaisseaux et on va avoir de nouvelles villosités
apparaître à partir des villosités préexistantes.
Il faut noté que certains bourgeons reste au stade syntitiotrophoblastique et se détache de la
villosité donc tombe dans la chambre intervilleuse. Quand ils sont passés dans la chambre
intervilleuse ils peuvent passé dans la circulation maternelle, drainé par les veines utérines.
En faite il y a des éléments syntitiotrophoblastiques qui circulent dans la circulation
maternelle et ceci a des conséquences pratiques : dès à présent on sait isolé cet ADN fœtale
dans le sang maternelle par une simple prise de sang et en pratique courante on peut dès 8
semaines de développement déterminé le sexe fœtal ou le groupe sanguin fœtal par des
techniques de génétique ; ceci est très important pour certaines maladies liés au chromosome
X qui ne survienne chez le garçon pour un cadre de diagnostique prénatale. Mais on s’est
aperçu en développant ces techniques que cet ADN de ces amas syntitiotrophoblastiques
persistaient pendant des années dans la circulation maternelle et ce qui pose problème c’est
quand une femme a eu plusieurs grossesses pour savoir si l’ADN qu’on a isolé est bien
l’ADN de cette grossesse là ou d’une grossesse antérieure. (Les femmes comme cela sont dit
des chimères au sens biologique du terme).
Ces villosités nouvelles, celles qui ont évolués complètement, soit elle reste libre dans la
chambre intervilleuse et ce sont des villosités « libres », soit elles adhèrent au
syntitiotrophoblaste attenant à la coque cytotrophoblastique externe pour constituer des
villosités « crampons » : on aboutit ainsi à la formation de véritables arbres villositaires.
Schéma : Ce qui tapisse la surface des villosités initialement libres c’est du
syntitiotrophoblaste, quand ces villosités s’approchent du placenta elles vont adhérer au
syntitiotrophoblaste qui borde le cytotrophoblaste de la coque cytotrophoblastique externe.
Passer le 2eme moi, les cellules cytotrophoblastiques se raréfient et cessent de constituer
un épithélium, ce sont des cellules isolées situés entre la membrane basale du trophoblaste et
le syntitiotrophoblaste et on leur donne le nom de Langhans. Ces cellules d’origine
cytotrophoblastique sont toujours capables de proliférer pour générer du syntitiotrophoblaste.

3
Remarquons que quand il n’y a plus de cytotrophoblaste on a diminué la distance entre sang
maternelle et sang fœtale, ce processus va se continuer : le mésenchyme va cesser de
s’interposer entre capillaires villositaires et le syntitiotrophoblaste et au 3eme trimestre de
grossesse on assiste à un accolement des membranes basales de l’endothélium des capillaires
villositaires et de la membrane basale trophoblastique. C’est à ce niveau là que la distance
minimale entre sang maternelle et sang fœtale est alors établit, elle est de l’ordre de 3,5
microns pour une distance initiale à la fin du premier moi de 20 microns. Et c’est à ce niveau
exclusivement que s’effectuent les échanges fœto-maternelles. Schéma : On voit que ce sont
que les endroits d’accolements des capillaires villositaires à la membrane basale
trophoblastique où se font réellement les échanges fœto-maternelles.
Ce développement des villosités est asymétriques et ce fait essentiellement au niveau du pole
embryonnaire pour former le chorion villeux alors qu’au pole antiembryonnaire les villosités
dégénèrent pour former le chorion lisse, au niveau du chorion lisse. L’accolement du
mésenchyme somatopleural du chorion lisse et du mésenchyme somatopleural qui borde la
cavité amniotique forme ce qu’on appel les membranes placentaires ou membranes
amniochoriales. Quand on dit qu’il y a rupture des membranes au cours de l’accouchement,
c’est l’ensemble de ces membranes qui sont rompues pour permettre l’évacuation du liquide
amniotique et ça précède de quelques minutes à quelques heures l’expulsion fœtale.
Donc chorion lisse + amnios c’est la membrane amniochoriales alors que l’association des
villosités choriales du pole embryonnaires à la muqueuse endométriales forment le placenta
proprement dit.
Ce placenta s’implante au niveau d’une partie de l’endomètre utérin et ce processus
d’implantation va profondément modifier cet endomètre et les différentes régions
endométriales qui vont se modifier prennent le nom de Caduque (tomber).
On distingue la caduque pariétal qui est situé en dehors de la zone de nidation et la caduque
ovaire ou ovulaire ou réfléchis qui est au contact du chorion lisse qui recouvre l’œuf et qui
sépare l’œuf de la lumière utérine dans laquelle il fait saillis. On conçoit que très rapidement
les deux caduques ovaire et pariétale s’accolent et fusionnent du fait de l’augmentation de
volume du fœtus et du liquide amniotique à l’exception de la zone du col utérin. Ce col est
obturé par un bouchon muqueux qui est élaboré par les glandes cervicales utérines et
l’éviction du bouchon muqueux est un des premiers signes qui annoncent le déclenchement de
l’accouchement : contractions qui permettent la dilatation du col et expulsion du nouveau né.
La « perte des os » c’est les membranes amniochoriales qui se rompent.
Il y a une 3eme caduque : la caduque basilaire situé entre chorion villeux et le myomètre. Elle
est formé d’une couche compact au contact du chorion et d’une couche spongieuse qui
contient les glandes de l’endomètre et les artères spiralées.
Rapports entre les villosités et la caduque basilaire.
Le syntitiotrophoblaste qui borde les villosités crampons est en continuité avec le
syntitiotrophoblaste qui borde la coque cytotrophoblastique externe (ce n’est qu’une
conséquence de leur mode de formation).
Les cellules cytotrophoblastiques des colonnes qui sont à la base des villosités crampons ont
un comportement particulier : Elles ont une intense activité de prolifération et forment le
cytotrophoblaste intermédiaire. Cette intense activité de prolifération lui permet de participer
à l’allongement de la villosité crampon en formant le syntitiotrophoblaste de cette villosité.
Ces cellules cytotrophoblastiques des colonnes sont aussi capables de migrer dans
l’endomètre pour former le cytotrophoblaste extravilleux. Ces cellules cytotrophoblastiques
extra villeuses : soit elles persistent dans la muqueuse utérine et se différencient en cellules
géantes bi ou trinucléés dispercées dans l’endomètre utérin mais surtout elles migrent vers la
paroi des artères utérines et deviennent endovasculaires avec des caractéristiques de cellules

4
endothéliales. Ces cellules deviennent endovasculaires avec formation de bouchons
intravasculaires et on pense que ces bouchons ont un rôle pour limiter la pression sanguine au
sein de la chambre intervilleuse. Ces cellules cytotrophoblastiques envahissent la paroi des
artères utérines puis détruisent partiellement les cellules musculaires de la paroi entraînant
une diminution des résistances vasculaires des artères spiralées. Le troisième rôle de ces
cellules cytotrophoblastiques extra villeuses et des cellules déciduales de l’endomètre utérin :
elles synthétisent une grande quantité de substances fibrinoide à l’interface entre la couche
compact et la couche spongieuse de l’endomètre et cette accumulation de substance fibrinoide
permet le clivage entre la plaque basale (couche compact) d’une part (celle qui est observable
après la délivrance placentaire à la surface du placenta) et le lit placentaire (couche
spongieuse) : celui qui va rester en place et se régénérer pour former l’endomètre normal en
dehors de la grossesse. A terme, la vascularisation utérine est assuré par environ une 100ene
d’artères spiralées (branches des artères utérines). Le débit sanguin de l’ensemble de ces
artères spiralées est d’environ 600mL/min (grande portion du débit cardiaque maternelle) et
comme le contenue de la chambre intervilleuse en sang maternelle est de l’ordre de 150mL au
cours du troisième trimestre de la grossesse, on en déduit que le contenu de la chambre
intervilleuse est renouvelé environ 4 fois par minute. Le fait qu’il y ait une grande quantité de
sang dans la chambre intervilleuse permet de protéger le fœtus ; néanmoins il faut savoir que
le défaut d’invasion cytotrophoblastique des artères spiralées est à l’origine d’une non
diminution des résistances vasculaires au niveau des artères spiralées et ça a une double
conséquence : hypertension artérielle maternelle et une diminution du flux sanguin à
destination de la chambre intervilleuse et c’est responsable d’une pathologie non rare (1 à 2%
des grossesses) qu’on appel la toxémie gravidique ou aussi pré éclampsie.
Placenta normal à terme.
Après l’expulsion ça se présente comme une galette ou gâteau placentaire (discoide). Ce
qu’on voit qui a été expulsé avec le placenta après la délivrance, c’est la plaque basale qui est
la partie dérivée de l’endomètre maternelle. Et sur le versant fœtal où s’implante le chorion,
c’est la plaque chorial.
Schéma : le sang fœtale arrive par les 2 artères ombilicales. Au niveau de la plaque chorial ils
vont donnés des tas de branches choriales des artères ombilicales qui vont assurer la
vascularisation de l’ensemble des villosités. Le sang des capillaires villositaires est drainé par
les veines choriales qui convergent vers la veine ombilicale. Ces villosités baignent au niveau
de la chambre intervilleuse, chambre intervilleuse qui est alimenté par les artères spiralées.
Le placenta normal à terme est :
- chorioallantoidien : Allantoïdien car la seul contribution de l’allantoïde c’est les 2
artères et la veine ombilicales qui sont dérivés du système vasculaire d’origine
allantoïdien.
- Hémochorial : car les villosités fœtales baignent directement dans le sang maternelle.
- Villeux : fait de villosités dont la surface globales à terme est d’environ 10 m².
- Discoïde : 20 cm de diamètre sur 3cm d’épaisseur.
- Pèse 500 g. (1/6 du poids du nouveau né à terme).
- Constitué de 20 cotylédons et chaque cotylédon est définit par une petite indentation
sur la face externe du placenta qui correspond à des septats (intercotylédonaires à
partir de la plaque basale) incomplets qui font saillis dans la chambre intervilleuse.
- Fonctions d’échange : respiratoire, nutritif et d’excrétion. En effet le rein fœtal n’a
pas de fonction excrétrices vis à vis du métabolisme fœtal. Mais il y a production
d’urine par le fœtus. A 14 semaines, ce sont les urines fœtales qui constituent tout le
liquide amniotique.

5
- Fonction endocrine : production d’HCG, de progestérone en quantité suffisante pour
maintenir la grossesse en absence de corps jaune.
- Synthétise aussi des oestrogènes qui favorisent la croissance de l’utérus et le
développement de la glande mammaire afin de nourrir l’enfant après sa naissance.
Circulation foetoplacentaire (point de vue du transport d’oxygène).
Le sang des capillaires villositaires qui s’est oxygéné au contact du sang maternelle est
drainer par la veine ombilicale et sa saturation en O2 est de 80% (la + forte). En effet le
placenta est une changeur imparfait car consomme une petite partie de l’O2. Ce sang veineux
ombilical se distribue au système porte hépatique mais surtout en majorité il se draine
directement par l’intermédiaire du ductus veinosus dans le système cave inférieur.
En amont de l’abouchement du ductus veinosus la saturation dans le système veineux cave
inférieur est très faible (car l’O2 est déjà extrait) et la saturation est de l’ordre de 26%.
En aval de l’abouchement du ductus veinosus, la saturation est de 67%. Ce sang qui vient de
la veine cave inférieur aboutit dans l’oreillette droite mais le trajet de veine cave inférieur est
telle qu’il se draine préférentiellement par le foramen oval vers l’oreillette gauche et de
l’oreillette gauche au ventricule gauche vers aorte ascendante vers les branches de la gerbe
aortique à destinée céphalique et des membres supérieurs ; la saturation dans ce territoire est
de 62% environ. Ce qui fait chuter la saturation entre la veine cave inférieur et les branches à
destinés céphaliques c’est qu’il y a un peu de sang de la veine cave supérieur qui rentre dans
l’oreillette gauche.
Pour la veine cave supérieur, le sang a aussi une saturation très basse (31%), il se draine dans
l’oreillette droite et préférentiellement dans le ventricule droit. Du ventricule droit il va dans
le tronc de l’artère pulmonaire et la saturation est d’environ 52%. Il n’y a que 10 à 20% du
flux du tronc de l’artère pulmonaire qui s’engage dans les branches de l’artère pulmonaire, le
reste va rejoindre l’aorte descendante par l’intermédiaire du canal artériel ou ductus artériosus
qui rejoint l’aorte descendante (c’est la région de l’isthme aortique). En aval de
l’abouchement du canal artériel, la saturation en O2 pour les branches de l’aorte descendante
est d’environ 58%. On remarque que la saturation en oxygène dans les branches à destinés
céphaliques est supérieur à la saturation dans les branches à destinés abdominales.
Formation des annexes chez les jumeaux dizygotes.
2 ovocytes fécondés par 2 spermatozoïdes distincts et qui s’implantent tous les deux
simultanément dans la cavité utérine donc pas plus de ressemblance que des frères et soeurs.
Chaque embryon (fœtus) va développer un placenta et des membranes amniochoriales qui lui
sont propre et on aboutit ainsi à des annexes dichoriales diamniotiques. Pour des raisons
d’encombrement, souvent ces membranes fusionnent ; plus exactement ce sont les caduques
réfléchis et les membranes amniochordiales qui fusionnent pour former une membrane
interovulaire épaisse.
Chez les jumeaux monozygote.
Sont des jumeaux génétiquement identiques qui résultent de la fécondation d’un seul ovocyte
par un seul spermatozoïde aboutissant à la formation d’un seul zygote qui va diviser
ultérieurement. Ce zygote se divise au stade 2 blastomères qui donnent naissance à 2
blastocytes ; chaque blastocyste donne naissance à un embryon et à ses annexes placentaires
et amniotiques et on aboutit comme pour les jumeaux dizygotes à une grossesse gémellaires
dichoriales diamniotiques. Quand au cours d’une grossesse on découvre que celle ci est
gémellaire dichoriales diamniotiques on peut pas dire sur ces seules données s’il s’agit de
jumeaux dizygotes ou monozygote sauf si le sexe est différent : là on pourra dire que c’est
dizygote.
 6
6
1
/
6
100%