2) Réhabilitation au moyen des aides auditives dans l`otite chronique

1
Prothèses auditives amplificatrice par voie non aérienne.
Eric TRUY (1,2), Stéphane GALLEGO (1,2), Didier BOUCCARA (3), Stéphane TRINGALI
(1,4),
1. Université de Lyon, Université Claude Bernard Lyon 1, INSERM U1028, CNRS UMR5292, Lyon
Neuroscience Research Center, Brain Dynamics and Cognition Team, F-69000, France
2. Hospices Civils de Lyon, Hôpital Edouard Herriot, Département d'ORL, de Chirurgie Cervico-
Maxillo-Faciale et d'Audiophonologie, F-69003 Lyon, France.
3. Assistance Publique–Hôpitaux de Paris, Hôpital Beaujon, Service d’ORL et de Chirurgie de la
Face et du Cou, F-92110 Clichy.
4. Hospices Civils de Lyon, Hôpital Lyon-Sud, Service d'ORL et d’Otoneurochirurgie, F-69495
Pierre-Bénite, France.
Correspondance :
Eric TRUY, département d’ORL, de Chirurgie Cervico-maxillo-faciale et d’Audiophonologie.
Hôpital Edouard Herriot. Place d’Arsonval. 69437 Lyon cedex 03. France
Tel : 00 (33) 4 7211 0555
Fax : 00 (33) 4 7211 0534
Courriel : [email protected]
Résumé :
La réhabilitation auditive par amplification ne repose pas seulement sur la voie aérienne. La voie
osseuse est possible depuis de très nombreuses années, classiquement par vibrateurs externes,
actuellement supplantés en tolérance et en efficacité par les possibilités liées à l’ostéointégration
d’un pilier sur lequel s’adapte un vibrateur. De manière plus récente le développement industriel des
Implants d’Oreille Moyenne (IOM) permet l’amplification par l’application directe d’une vibration
sur la chaîne ossiculaire, une ossiculoplastie ou la fenêtre ronde. Ces IOM employant soit la force
électromagnétique, soit la force piézo-électrique, ont vu leur champ d’application s’étendre des
surdités neurosensorielles vers les surdités de transmission ou mixtes. Le clinicien dispose ainsi de
nombreuses possibilités de réhabilitation n’utilisant pas la voie aérienne pour des indications très
larges. La connaissance des indications, des limites, des contraintes et des résultats est indispensable

2
de manière à offrir aux patients des capacités d’adaptation audioprothétique les plus appropriées et
efficaces.
Summary :
Today amplification is not only using air conduction. Bone conduction is well known since many
years classically using external vibrating devices The concept of osseointegration led to apply
vibration directly onto the skull bone bypassing the skin barrier, allowing better tolerance and
efficiency. More recently, industrially available devices have been developed using transducers
applying mechanical forces directly onto ossicles, ossicular prosthesis or round window membrane.
Forces are employed are either piezoelectic or electromagnetic. These Active Middle Ear Implants
can be used in a large variety of audiological and anatomical situations; fields of application
widening from historical indication of sensorineural Hearing losses to conductive or mixt hearing
losses. ENT and audiologists do need to know about indications, contra-indications, limits,
constraints and results, for best counselling and offering the best rehabilitation mode to patients.
Mots clés : Surdités. Prothèses auditives. Conduction osseuse. Ostéointégration. Implants auditifs
actifs. Stimulation électromagnétique. Stimulation piézoélectrique. Vibroplastie. Mono-Pseudo-
Stéréophonie.
Key words : Hearing losses. Hearing aids. Bone conduction. Osseointegration. Active Middle Ear
Implants. Electromagnetic stimulation. Piezoelectric stimulation. Vibroplasty. Mono-Pseudo-
Stereophony

3
Plan :
Introduction
1. Les différents systèmes :
1.1. Voie osseuse
1.1.1. Les vibrateurs externes :
1.1.2. Les appareillages partiellement implantés :
1.2. Implant d’oreille moyenne
1.2.1. Les systèmes électromagnétiques
1.2.2. Les systèmes piézoelectriques :
2. Indications
2.1. De la voie osseuse
2.1.1. Les surdités de transmission
2.1.2. La cophose unilatérale :
2.2. Des Implant d’oreille moyenne
3. Résultats
3.1. De la voie osseuse avec ostéo-intégration
3.1.1. En cas de surdités de transmission :
3.1.2. En cas de cophose unilatérale :
3.2. Des Implant d’oreille moyenne :
3.2.1. En cas de surdités neurosensorielles :
3.2.2. En cas de surdités de transmission et mixtes
Conclusion

4
Introduction :
L’amplification est à la base de la restauration fonctionnelle de nombreuses pertes auditives lorsque
la copho-chirurgie n’est pas possible ou à échoué, ou en cas de refus d’une telle chirurgie de la part
du patient. Si de nombreux patients tirent bénéfice des progrès de l’amplification par voie aérienne,
certains ne peuvent pas y avoir accès, ou bien la refusent, ou bien en vivent les limites. Ainsi il y a
une place pour l’amplification par voie osseuse et pour l’amplification directe au moyen d’un
caténovibreur implanté. Le développement rapide et important des technologies rend l’actualisation
de ce chapitre nécessaire.
1. Les différents systèmes :
1.1. La voie osseuse
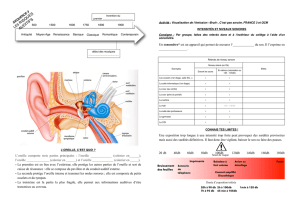
Le principe de l’amplification par voie osseuse repose sur la capacité à transmettre une information
auditive aux liquides cochléaires par ébranlement de la boîte crânienne. Il existe plusieurs théories
sur le principe de la transformation de l’onde vibratoire osseuse en perception auditive. La plus
plausible repose sur le fait, que l’oreille interne est en partie constituée d’un os dense entouré d’une
structure osseuse plus souple, la mastoïde (os pneumatique). Lorsque l’on vient faire vibrer le crâne
(qui est un os dense), l’élasticité de la mastoïde vient transmettre la vibration à l’oreille interne,
comme le ferait une masse flottante. Cette énergie transmise et emmagasinée par le couple
mastoïde/oreille interne vient mettre en mouvement les liquides cochléaires et ainsi transmettre et
transformer l’onde vibratoire en influx nerveux.
L’appareillage en conduction osseuse, classiquement par branches de lunettes vibrantes appliquées
sur les apophyses mastoïdes relativement peu utilisés, a vu son intérêt relancé par l’apparition des
systèmes dits ¨ostéo-intégrés¨ basés sur la biocompatibilité du titane au contact du tissu osseux.
1.1.1. Les vibrateurs externes :
Les branches de lunettes (figure 1): l’extrémité de la branche de lunette équipée d’un vibrateur,
vient se placer au contact de la mastoïde, transmettant directement le signal à l’oreille interne.
Les contours avec serre tête (figure 2) reprennent le même principe, mais sont très rarement utilisés
sauf chez les très jeunes enfants se présentant avec une atrésie auriculaire bilatérale. Ces prothèses
par conduction osseuse sont contraignantes et nécessitent un serrage appuyé sur la peau mastoïdienne
pour être efficaces ; elles sont employées jusqu’à ce que la croissance de l’épaisseur de la voûte
crânienne puisse admettre un pilier ostéo-intégré et transcutané pour adapter un vibrateur externe
(type BAHA « Bone Anchored Hearing Aid »).
Le soft Band BAHA (figure 3) est une bande élastique réglable adaptée autour du crâne, sur laquelle
est ajustée un adaptateur qui permet de clipper la partie externe d’une BAHA, ou un système
Sophono ou Ponto.
1.1.2. Les appareillages partiellement implantés :
La prothèse stimule directement la cochlée via l’os crânien sans l’atténuation de la barrière cutanée
car le vibrateur est directement couplé à une partie ostéo-intégrée.
Le système BAHA® (Bone Anchored Hearing Aid) (Cochlear Acoustics Ltd, Lane Cove,
Australie) (figures 4a et b) est l’appareillage historiquement commercialisé en premier en 1977. La
prothèse BAHA comporte un système électronique contenu dans un boîtier, fixé sur un pilier en
titane lui même vissé sur un implant en titane ostéo-intégré. Il existe quatre types de boîtiers, la
BAHA® Divino®, le BAHA® Intenso®, la BAHA® Cordelle II, et la nouvelle BAHA BP100
disponible depuis 2010. La BAHA® Divino® a remplacé le BAHA® Classic 300 et la BAHA®
Compact. Elle offre un traitement numérique des signaux et un microphone directionnel. La BP100

5
dispose d’un réducteur de bruit, de 2 micros multidirectionnelles multibandes autoadaptatifs, d’un
système anti Larsen et se règle selon comme une aide auditive numérique avec une possibilité
d’adapté le gain pour chaque fréquence. Toutes les BAHA se fixent sur le pilier par un système de
type bouton-pression. La fixture est composée d’une vis en titane de 3 ou de 4 mm pour le modèle
standard ; c’est elle qui est vissée dans l’os temporal et soumise à ostéo-intégration. Le pilier est
fabriqué en titane et vient se visser sur la fixture. Un système pré monté est désormais proposé de
pilier BAHA® (système BAHA® FAST) [1]. Il existe également depuis 2011, une nouvelle vis
proposée par Cochlear qui permettrait d’obtenir une meilleure tolérance cutanée et un temps
d’ostéointégration plus court.
Toutes les techniques chirurgicales décrites sommairement dans ce chapitre sont développées dans
le chapitre de l’EMC consacré aux techniques d’implantation en otoneurochirurgie [2].. Le geste
chirurgical d’implantation BAHA fait appel en général à une technique en un temps ; elle est réalisée
chez l’adulte le plus souvent sous anesthésie locale, sous anesthésie générale chez l’enfant. Le site
d’implantation est repéré de manière à éviter tout contact ultérieur de la prothèse avec l’hélix. La
situation idéale est à 55mm du centre du conduit auditif externe (CAE). Le scalp au niveau du site
d’implantation est tondu, le marquage du site d’implantation et du lambeau cutané effectué. Après
infiltration, on effectue la taille du lambeau, idéalement au moyen d’un minidermatome ce qui va
assurer la mensuration en largeur et la taille en épaisseur emportant les follicules pileux. Si on ne
possède pas de minidermatome on utilisera la technique dite « manuelle » [3]. ; un lambeau cutané
est réalisé au bistouri à lame froide par une incision jusqu’au plan périosté et dans l’épaisseur du
derme en sectionnant les follicules pileux de telle manière que la peau devienne glabre et que
l’épaisseur du lambeau soit d’environ 1mm. L’exérèse du tissu cellulaire sous cutané sur toute la
zone où viendra s’appuyer le boîtier doit déborder au delà de l’incision cutanée, de manière à assurer
ultérieurement un aspect émoussé en cuvette de la zone circonscrivant le pilier. Au centre de cette
zone on réalise un avant trou par la fraise guide de 3mm sous irrigation constante de manière à
refroidir l’os pour ne pas compromettre l’ostéointégration de la vis. Si l’épaisseur est suffisante on
retirera la garde da le fraise guide ce qui permet de poursuivre le fraisage jusqu’à 4mm de
profondeur. Chez les adultes il est possible d’aller jusqu’ à 4mm ; chez l’enfant il est nécessaire de
ne pas dépasser de 3mm. Cet avant-trou sert à réaliser un trou plus large à l’aide d’une fraise forêt ;
là encore l’irrigation abondante est capitale. Le système Fast avec vis autotaraudante permet à
l’implant monté sur le pilier d’être mis en place directement ; le moteur est réglé à faible vitesse avec
un couple de force adapté. Le lambeau cutané est remis en place, une pastille cutanée est déposée
exactement au dessus du site d’implantation avec un punch pour biopsie de 4mm. Le pilier est
ressorti à travers la peau. On effectue ensuite la fermeture de l’incision cutanée. Un feuillet de
biotulle est maintenu sur le site d’implantation par un capuchon plastique clipé sur le pilier. Les
points sont enlevés ainsi que le feuillet entre la plaie et le capuchon, aux environs du dixième jour.
L’adaptation prothétique et les réglages sont réalisés une fois l’ostéo-intégration obtenue (plus de
deux mois après l’opération).
La technique en deux temps est elle recommandée pour les enfants par quelques auteurs, pour les os
irradiés, pour les patients pour lesquels un implant est mis en place en même temps qu’est effectuée
une chirurgie d’exérèse de neurinome de l’acoustique, ainsi que les patients dont la qualité osseuse
ne parait pas optimale. L’intervention est débutée de la même façon, un implant est inséré sans
connexion à un pilier, une vis de couverture est placée afin de protéger le filetage interne à l’implant
dans lequel serra vissé le pilier ultérieurement, d’une invasion tissulaire. Le second temps est réalisé
trois à six mois plus tard. La découpe cutanée permet de découvrir l’implant, de retirer la vis de
couverture et de mettre en place de pilier.
Chez le très jeune enfant il est possible de réaliser des implantations avant l’âge de cinq ans, avec
une corticale osseuse d’épaisseur inférieure à 2.5mm. Cette intervention est préconisée en deux
temps [4]. Dans certains cas une vis de 3mm n’est pas utilisable en raison d’une faible épaisseur
osseuse. Pour augmenter le volume osseux, certains auteurs proposent un artifice qui consiste à
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%