CHIMIE Chapitre : MOLECULES Objectifs :

CHIMIE
Chapitre : MOLECULES
Objectifs :
- Identifier les atomes constitutifs d’une molécule.
- Représenter quelques molécules par leur modèle moléculaire.
- Modèle de Lewis de quelques molécules (règle de l’octet)
- Calculer une masse molaire moléculaire.
L’eau est un produit mais on ne le trouve pas dans la classification périodique. Pourquoi ?
1. Définition.
Une molécule est ………………..………………..……………………………………………….
……………………………………..…………………………………………………………………
Une molécule est ……………………………………..………………… .
Chaque molécule a une ……………………….……….…… qui indique le …………………… de
chaque atome la composant avec, en indice, le …………………….. de chaque type d’atome.
Exemple : molécule d’eau
La formule brute de la molécule d’eau est H20. Elle est composée de :
.……………………………………………….
…..…………………………………………….
Exercice : compléter le tableau.
NOM
FORMULE
COMPOSITION
dioxygène
O2
Dioxyde de Carbone
CO2
Acétone
C3H6O
calcaire
CaCO3

CHIMIE
2. Modèles moléculaires.
Les molécules peuvent être représentées par des modèles moléculaires.
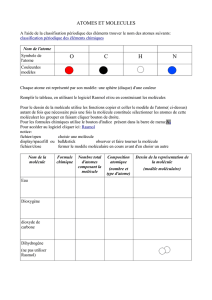
Les atomes sont modélisés par des boules colorées.
Type
d’atome
Hydrogène
H
Carbone
C
Oxygène
O
Chlore
C
Azote
N
couleur
blanc
noir
rouge
vert
bleu
A l’aide des modèles moléculaires, construire chaque molécule du tableau suivant et compléter :
Molécule
formule brute
composition
modèle
moléculaire
schéma de la
molécule
eau
H2O
2 atomes d’hydrogène
1 atome d’oxygène
2 boules blanches
1 boule rouge

CHIMIE
Chapitre : MOLECULES
3. MASSE MOLAIRE MOLECULAIRE .
RAPPEL : vu dans le chapitre 2 : la masse molaire atomique est la masse d’une mole d’atomes.
Elle est donnée par la classification périodique . On la note M.
Son unité est : g/mol.
Exemple : A l’aide de la classification périodique, répondre aux questions :
Quelle est la masse molaire atomique du carbone? …………………………
Quelle est la masse molaire atomique du fer ? …………………………
Quelle est la masse molaire atomique de l’hydrogène ? …………………………
La masse molaire moléculaire est la masse molaire d’une molécule.
…………………………………………...………………………………………………………..
…………………………………………...………………………………………………………..
…………………………………………...………………………………………………………..
Exemple :
Molécule du chlorure de sodium: NaC
…………………………………………...………………………………………………………..
……………………………...………………………..……………………………………..
Molécule d’eau : H2O
…………………………………………...………………………………………………………..
……………………………...………………………..……………………………………..
Molécule de l’oxyde de fer : Fe3O4
…………………………………………...………………………………………………………..
……………………………...………………………..……………………………………..
1
/
3
100%