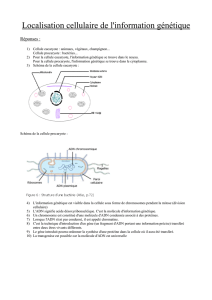
Recherche de QTL chez le poulet

Génétique appliquée D. Locker Semestre 5
1
Génétique appliquée
Sommaire
I. Délétions .......................................................................................................................................... 3
A. Localisation des gènes par les délétions ..................................................................................... 3
II. Inversions ........................................................................................................................................ 5
A. Souches létales balancées ........................................................................................................... 5
I. Mutagenèse ..................................................................................................................................... 9
A. Mutagénèse réalisée pour trouver des mutations affectant le développement chez la
drosophile ............................................................................................................................................ 9
B. Mutagénèse utilisant des éléments transposables chez la drosophile ..................................... 10
C. Principe de la récupération d’un plasmide ............................................................................... 13
D. Système enhancer trap ............................................................................................................. 13
E. Système Gene trap .................................................................................................................... 14
F. Systèmes permettant la surexpression des gènes .................................................................... 14
II. Transgénèse................................................................................................................................... 17
A. Limite de l’utilisation de P : le transposon ne s’insère pas au hasard. Solution : utiliser de
nouveaux transposons ...................................................................................................................... 17
III. Clones mitotiques ...................................................................................................................... 17
A. Production des crossing over mitotiques et mise en évidence de clones mitotiques .............. 17
B. Souris ......................................................................................................................................... 19
1. Mutagenèse ........................................................................................................................... 19
2. Cellules ES et recombinaison ................................................................................................. 21
3. Utilisation des éléments transposables pour la mutagenèse chez la souris ......................... 26
C. Mutagenèse chez le poisson zèbre Danio rerio......................................................................... 26
D. Analyse génétique chez Caenorhabditis elegans ...................................................................... 28
I. Histoire de l’interférence ARN ...................................................................................................... 31
II. Définitions ..................................................................................................................................... 31
III. Les publications ......................................................................................................................... 31
IV. 1999 : Le mécanisme ................................................................................................................. 32
V. 2000 : découverte de la machinerie .............................................................................................. 32
VI. Importance de la découverte .................................................................................................... 32
VII. RISC ............................................................................................................................................ 33
VIII. Activation du siRNA ................................................................................................................... 33

Génétique appliquée D. Locker Semestre 5
2
IX. Méthodes pour produire le siRNA ............................................................................................. 33
I. Le polymorphisme des protéines : Séparation des protéines par électrophorèse ....................... 37
II. RFLP ............................................................................................................................................... 38
III. Les VNTR (Variable Number Tandem Repeats) ......................................................................... 42
IV. RAPD (Randomly Amplified Polymorphic DNA) ........................................................................ 45
V. AFLP (Amplified Fragment Length Polymorphism) ....................................................................... 46
VI. SNP (Single Nucleotide Polymorphism) ..................................................................................... 48
I. Histoire .......................................................................................................................................... 51
II. Principe de l’obtention des empreintes génétiques ..................................................................... 51
III. Identification des restes des Romanoff ..................................................................................... 54
IV. Exemple de l’utilisation des tests ADN dans le cadre d’un crime – USA versus Raymond Jenkins
56
Recherche de QTL chez le poulet .......................................................................................................... 70
A. Approche génétique : approche QTL ........................................................................................ 70
B. Répertorier l’ensemble des gènes des régions QTL .................................................................. 71
C. Choisir les bons candidats ......................................................................................................... 71

Génétique appliquée D. Locker Semestre 5
3
Utilisation en génétique formelle des
accidents chromosomiques
I. Délétions
A. Localisation des gènes par les délétions
La délétion est une perte de matériel génétique dans un segment AB, ou CD par exemple. Le
chromosome diminue de taille. Il y a alors appariement avec formation d’une boucle. Si l’on met un
chromosome normal en face d’un chromosome qui porte CD, toute mutation en face récessive
s’exprime chez le diploïde. C’est ce qu’il se passe chez le male drosophile. On connaît l’espace parti
au niveau de la délétion, donc si une mutation s’exprime après la délétion, ça veut dire qu’elle se
localise entre les deux extrémités de la mutation.
Les travaux de Benzer : il a mis en place l’idée du triplet pour le code génétique. Il a aussi travaillé sur
ces délétions.
Le but de Benzer était d’avoir un maximum de mutants, et de les muter.
RIIA1 x RIIA2
B distance A1 et A2 =
P RIIA1 R RII+
RIIA2 RIIA1 RIIA2

Génétique appliquée D. Locker Semestre 5
4
M1 Gène RII M2
Génome T4
Délétion 1
Délétion 2
Délétion 3
Croissance
M1 x del1 K – – M2
M1 x del2 K + – M2
M1 x del3 K + – M2
On peut déterminer la position de la délétion au nucléotide près. Ce qui est possible chez le
bactériophage est possible chez l’homme.
C’est avec cette technologie que l’on a localisé le gène de la dystrophie musculaire de Duchesne dans
la région P17 du chromosome X.
A
B
C

Génétique appliquée D. Locker Semestre 5
5
Pour récupérer beaucoup de ||, on met en excès le chromosome normal. Pour éliminer les DNA
verts. Ensuite, on met les DNA verts en excès, pour diminuer l’appariement en blanc.
Toutes les manipulations sont corrélées au fait que l’on connaît parfaitement les délétions que l’on
utilise. Les croisements ont eu lieu pour déterminer les bornes des délétions.
II. Inversions
Même séquence d’ADN, mais pas dans le même ordre.
Les inversions jouent le rôle d’inhibiteur de la recombinaison. Les produits de la recombinaison dans
l’inversion sont complètement inviables.
A. Souches létales balancées
Une souche a un chromosome avec une mutation létale, et sur l’autre chromosome une autre
mutation létale récessive.
Cy inversion L+ mv
[CyL] x
Cy+ L m
// Voir « Les souches létales balancées »
// Voir « exemple de l’utilisation des souches létales balancées… ».
Plutôt que de compter, on utilise les souches létales balancées. La mutation est sur le chromosome 2
(première solution) : // voir diapo.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
1
/
71
100%