Travaux Pratiques de Biologie Molculaire 2004-2005 Licence

Travaux Pratiques de Biologie Moléculaire 2007-2008 Licence Semestre 5 S. BOURGERIE
Module: Régulation de l’expression du génome – SC-L5-BH05
- TRAVAUX PRATIQUES -
REGULATION DE L’EXPRESSION DES GENES CHEZ LES PROCARYOTES
(3 séances de 5h)
Plan des expériences :
Jour 1 : croissance bactérienne / expériences d’induction
Jour 2 : évaluation activité β-galactosidase / mutagenèse aux UV
Jour 3 : analyse des résultats
QUELQUES RECOMMENDATIONS
Se munir d’une blouse, d’un marqueur noir indélébile et d’une montre avec une « trotteuse » (ou mieux un chronomètre) .
Le travail pratique est à faire individuellement et avec soin.
Le compte-rendu est à remettre à l’issue de la dernière séance.
Régulation du taux de synthèse de la β-galactosidase chez
Escherichia coli
Introduction
Le lactose est un disaccharide composé d'une molécule de D-galactose et d'une molécule de D-glucose unies par
une liaison β1-4. La β-galactosidase est une hydrolase qui coupe spécifiquement la liaison β1-4 du lactose.
L'activité de cette enzyme peut être mesurée en utilisant un galactoside, l'ortho nitrophényl β-D-galactoside
(ONPG), substrat de la β-galactosidase dont l'action libère de l'ortho-nitrophénol (ONP), coloré en jaune. Le
système génétique gouvernant le métabolisme du lactose chez E. coli comprend 3 gènes de structure groupés en
un opéron.
organisation de l'opéron lactose :
Un opéron est défini comme une série de gènes adjacents dont la régulation est coordonnée (c'est à dire que si
l'un des gènes est off, les autres le sont aussi) ; c'est un système seulement retrouvé chez les procaryotes.
L'opéron lac comprend 3 gènes (lacY, Z et A) précédés par un seul et même promoteur et un opérateur.
Lac Z code la β-galactosidase, enzyme qui catalyse l'hydrolyse du lactose en glucose et galactose ; LacY code une
perméase, une protéine qui siège dans la membrane cellulaire et qui facilite l'entrée du lactose dans la cellule ;
LacA code une transacétylase dont la fonction n'est pas connue.
Deux de ces trois gènes (et peut être aussi le troisième) doivent par conséquent être régulés avec le métabolisme
du lactose; donc selon les conditions nutritionnelles être on ou off.
régulation de l'opéron :
Le glucose pour E. coli constitue sa source de carbone favorite; si du glucose est présent, E. coli ignore les autres
sucres. E. coli a besoin des enzymes de l'opéron lac lorsque du lactose est présent mais pour elle il n'y a pas plus
facile à métaboliser que le glucose. Quand le lactose n'est pas présent, il n'est pas nécessaire que l'opéron lac
s'exprime; la répression de l'opéron lac se réalise par l'action d'un répresseur lequel se fixe à l'opérateur de
l'opéron lac empêchant ainsi toute transcription. Le répresseur lac est codé par le gène lacI lequel est situé à
proximité de l'opéron lac sans appartenir à celui ci. Le lactose se fixe au répresseur et empêche celui-ci de
réprimer l'opéron.
L'IPTG (isopropylthiogalactoside) est un analogue du lactose qui se fixe aussi au répresseur mais contrairement
au lactose ne nécessite pas la lac perméase pour rentrer dans la cellule. Parce que l'IPTG est plus hydrophobe que
le lactose (du fait du groupement isopropyl) elle passe au travers des membranes.
Principe du dosage de la
β
-galactosidase
L'ortho-nitrophényl-β-D-galactopyrannoside (ONPG) est un analogue du lactose qui peut être hydrolysé par la
1

β-galactosidase en galactose et o-nitrophénol. L'ONPG est incolore tandis que l'o-nitrophénol est jaune avec un
maximum d'absorbance autour de 420 nm.
Le SDS et le dichloroéthane sont ajoutés au mélange d'essai afin de casser les cellules. Ceci permet à l'enzyme et
au substrat de se « retrouver ». L'addition de ce détergent et de ce solvant organique n'affecte pas l'activité de la
β-galactosidase. De nombreuses enzymes (dont la β-galactosidase) préfèrent des conditions réductrices pour
fonctionner (ceci est assuré par l'addition de β-mercaptoéthanol dans le mélange essai).
Le pH optimum d'activité de la β-galactosidase se situe à environ 7,0. Cette enzyme ne fonctionne pas aux pH
extrêmes; aussi l'addition de carbonate de sodium amenant le pH au delà de 9,0 permet à la réaction en cours
d'être immédiatement arrêtée. L'absorbance mesurée sur une suspension bactérienne est proportionnelle au
nombre de bactéries présentes (à condition que la densité en bactéries ne soit pas trop importante).
But de l'expérience :
L'expérience a pour but de provoquer l'induction de l’expression du gène lacZ en utilisant différents agents
inducteurs, naturels ou artificiels et ceci pour différentes densités bactériennes (suivi au cours du temps).
L'évaluation de l'induction se fera par la mesure de l'activité β-galactosidase en utilisant un substrat synthétique,
l'ONPG.
Dans les manipulations, il sera utilisé la souche E. coli BL21(DE3).
Mutagenèse de l’opéron lactose
Si l’on fait croître E. coli exponentiellement, une cellule donne végétativement naissance à de multiples
descendants tous identiques au parent d’origine. Mais de temps en temps, avec une fréquence de l’ordre de 10-7-
10-8 par cellule et par génération, il apparaît une cellule qui diffère du type parental par un caractère donné. Cet
organisme est appelé mutant et le type parental type sauvage. Le mutant peut être aussi stable que le type
sauvage ; il peut en différer par la résistance à un antibiotique donné, par la morphologie de ses colonies, par le
besoin en un facteur de croissance exogène, par sa résistance à un bactériophage donné, par l’incapacité à
fermenter tel ou tel sucre etc.
Il est possible d’augmenter le taux de mutation spontanée par action de mutagènes chimiques ; d’autres agents
mutagènes existent, comme les rayonnements ultraviolets.
Il est relativement simple à partir de très grandes populations bactériennes, d’isoler des mutants qui peuvent se
multiplier dans un milieu où la souche parente ne se multiplie pas. Par exemple des mutants résistants à des
agents chimiques inhibiteurs de la croissance : il suffit d’étaler un grand nombre de bactéries sur une boîte de
Petri contenant l’agent toxique ; la méthode est totalement sélective : seul le mutant désiré pourra se multiplier et
donner naissance à des colonies.
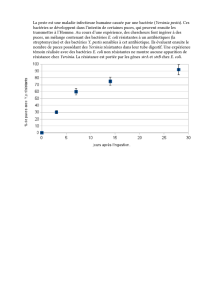
L’objectif des manipulations réalisées est d’obtenir des mutants de la bactérie E. coli qui expriment de manière
constitutive l’opéron lac ; chez ces mutants, sans ajout d’un inducteur, il y a expression de l’opéron lac.
L’obtention des mutants se fera soit par exposition aux UV (mutagenèse aléatoire) soit en utilisant un milieu de
sélection.
Evaluation de la croissance d’Escherichia coli
La bactérie Escherichia coli est un outil essentiel en biologie moléculaire, après avoir été le micro-organisme
de choix pour les études biochimiques et génétiques chez les procaryotes.
Cette bactérie se prête à la « transformation », c'est-à-dire, qu'après un traitement au CaCl2 par exemple,
elle devient « compétente » : capable d'accepter l'ADN plasmidique exogène que l'on souhaite amplifier. Il
apparaît donc indispensable de savoir manipuler ce micro-organisme et en premier lieu de savoir le cultiver. La
croissance se définit comme l'augmentation de la taille des bactéries puis de leur nombre.
L'évaluation de la croissance bactérienne peut se faire par :
- numération de colonies bactériennes sur milieu solide.
Un aliquote de la culture de bactéries est prélevée à différents temps et étalée sur une gélose nutritive
coulée dans une boîte de Pétri. Après incubation une nuit à 37°C, chaque bactérie engendre une colonie qui
constitue sa descendance, visible à l'œil nu.
- turbidimétrie de la culture bactérienne.
Un aliquote de la culture de bactéries est prélevée à différents temps. On mesure l’absorbance de la
suspension au spectrophotomètre dans le visible à 600 nm. L'absorbance (Abs) est proportionnelle au nombre de
bactéries par ml dans les limites : 0,1 < Abs600 < 1,0.
2

Abs.
600
= k Nb bact./ml
La valeur de k est une constante pour une bactérie donnée cultivée dans des conditions définies. Cette
relation s'établit en couplant la mesure de l’absorbance avec une numération sur milieu solide pour l’absorbance
mesurée.
L'expression mathématique de la croissance est :
Nt2 = Nt1 2µ(t2-t1) ou encore Abst2 = Abst1 2µ(t2-t1)
avec Nt = nb de bactéries au temps t
N
o = nb de bactéries au temps 0 de l'expérience
µ = nb de divisions par unité de temps.
Si pendant le temps t, la population double (Nt = 2N0), t représente alors le temps de génération t =1/µ. µ est le
taux de croissance ou nombre de divisions par heure.
La valeur de µ est une constante pour une bactérie donnée cultivée dans des conditions définies.
La courbe de croissance bactérienne est généralement caractérisée par une succession de phases :
- phase de latence µ = 0
- phase exponentielle µ > 0
- phase stationnaire µ = 0
- phase de mortalité µ < 0.
Les expériences d’induction et le suivi de la croissance d’
E. coli
sont menés conjointement :
une seule et même manipulation est réalisée.
Réactifs et matériel
Souche : E. coli BL21
Milieux de culture : milieu LB (+/- agar) (pour 1 litre: Tryptone 10g, Extraits de levure 5g et NaC1 10g) ; milieu M63 (pour
1 litre : 2g (NH4)2SO4, 13,6g KH2PO4, 0,5mg FeSO4 – pH7,0 + 1mM MgSO4 + 0,2 à 0,5% source carbonée (glycérol ou
mélibiose))
Produits chimiques : IPTG : 100 mM dans l'eau
Lactose : 8% dans l'eau
ONPG : 4 mg/mL en tampon phosphate de sodium 0,1 mol/L pH 7,0 (Mr = 301,3 ; une
solution à 4mg/mL correspond à 13,3 mM)
Tampon phosphate de sodium : Na2HPO4-NaH2PO4 0,1 mol/L pH 7,0
Tampon Z : 50 mM β-mercaptoéthanol (2-ME) ; 100 mM phosphate de sodium pH 7,0; 10 mM
KCl ; 1 mM MgSO4
Carbonate de sodium : 1 M dans l'eau
SDS : 0,1%
Dichloroéthane
(solution commerciale de 2-ME : d = 1,12 ; Mr = 78,13)
Manipulations
Cette étude de la régulation du taux de synthèse de la
β
-galactosidase chez Escherichia coli est réalisée par une série d'expériences menées sur 2 jours
consécutifs.
Au jour 1 : suivi de la croissance bactérienne et expériences d'induction
Au jour 2 : dosage de l'activité β-galactosidase
Toute manipulation de bactéries doit se faire stérilement, c'est-à-dire dans un diamètre de 20
cm autour de la flamme d'un bec Bunsen, avec du matériel stérile chaque fois que cela est
précisé.
Au jour 1
1- Evaluation de la croissance bactérienne à 37°C par turbidimétrie
- Transférer stérilement 20 ml de milieu de culture (milieu M63 + glycérol + MgSO4) dans un erlen de
100 ml.
- Ensemencer stérilement les 20 ml à partir d’une préculture
E. coli
BL21 , avec un volume qui
vous sera indiqué au début du T.P. Agiter modérément.
- Prélever immédiatement 1 ml de suspension, le mettre dans une cuve de spectrophotomètre
- Placer très rapidement l'erlen dans le bain agitateur thermostaté à 37°C. Noter l'heure
3

- Lire l'absorbance à 600 nm. (vérifiez périodiquement le zéro de l’appareil)
- Répéter le prélèvement et la mesure après 30 minutes et 60min.
- Reporter les valeurs de l'absorbance dans un tableau.
- L’absorbance, mesurée à 600nm, avant les expériences d’induction doit impérativement
atteindre la valeur de 0,400 (A600 >0,4).
Il faut attendre entre 45 et 60min pour atteindre l’absorbance désirée.
2- Expériences d’induction
- lorsque l’absorbance mesurée atteint au minimum la valeur de 0,4 (à 600nm), l’expérience
d’induction peut commencer.
- 2 expériences d’induction en parallèle sont menées :
soit l’expérience 1 (addition de lactose uniquement) soit l’expérience 2 (addition d’IPTG). Un témoin de
non induction est à prévoir.
ceci est fait pour 6 temps de cultures, c’est-à-dire à 0, 30, 60, 90, 120 & 150min d’induction.
- dans l’erlen utilisé, ajouter selon les cas
1- 60µl d’IPTG 100mM
2- 1520µl de lactose 8%
- après addition de l’inducteur, dans chacun des cas, bien mélanger le contenu du récipient
- prélever immédiatement 1ml de la suspension bactérienne dans l’erlen pour le mettre dans un tube
eppendorf clairement identifié (t0); placer l’échantillon aussitôt dans la glace
- replacer l’erlen dans l’agitateur thermostaté ; relever le temps
- réaliser les mêmes opérations toutes les 30min jusqu’au temps 150min d’induction (maintenez les
échantillons dans la glace, juste après le prélèvement)
- pour les temps 60, 90, 120 & 150min prélever 2 fois 1ml
Pour le temps 90 min, prélever
en plus
, 0,5 ml de suspension, le mettre dans un tube eppendorf stérile noté 0 (zéro).
- en parallèle n’oubliez pas de (toujours) réaliser les mesures d’A600nm
- en fin d’expérience, vous disposez d’une série de tubes (10 au total) correspondant aux différents
prélèvements effectués
- centrifuger tous les tubes (2min, vitesse max.) ; éliminer avec soin le surnageant (sans entraîner le
culot)
- laver les culots par 500µl de tampon phosphate : attention à ne pas perdre le culot !!
- stocker vos bactéries au froid pour le jour n°2 (congélation des culots)
3- Numération sur milieu solide
PENDANT LES TEMPS MORTS DE LA PREMIERE EXPERIENCE
- Préparer 7 boîtes de Pétri : noter sur la tranche du contenant (sans les ouvrir):
votre nom (PAS D'INITIALES) et le contenu prévu (n° de dilution)
- Couler par boîte 15 ml (minimum) de milieu nutritif gélosé LB maintenu en surfusion à 50°C.
- Bien faire sécher chaque boîte
- Préparer une série de tubes eppendorf stériles numérotés de 1 à 7
- Introduire 450 µl de milieu de culture LB stérile dans chaque tube.
- A partir de votre tube eppendorf 0 (correspondant au prélèvement réalisé à t90min), réaliser des
dilutions en série au 1/10ème comme suit:
- Homogénéiser le tube 0 par aspiration/refoulement
- Transférer 50 µl dans le tube 1; homogénéiser (par aspiration/refoulement)
- Transférer 50 µl du tube 1 dans le 2 ; homogénéiser etc... jusqu'au tube 7.
- A l’aide de billes de verre stériles, procéder aux étalements sur boite de Pétri selon les
indications qui seront fournies en TP.
- Les 3 dernières dilutions sont étalés (10-5, 10-6 et 10-7) ; à raison de 100µl par boîte, à faire en
double
- Incuber les boîtes ainsi ensemencées, retournées, une nuit à 37°C
La 7ème boîte sert de « boîte de secours ».
4

4- recherche de mutants bactériens exprimant de manière constitutive l’opéron lactose
OBJECTIF : obtenir une souche mutante d’E. coli BL21 pour laquelle l’expression de l’opéron lac se trouve
déréprimée : c’est à dire que la répression exercée par LacI ne se produit plus.
Pour cela, la souche sauvage est cultivée sur milieu minimum contenant comme seule source de carbone du
mélibiose et à la température de 42°C.
E. coli possède une perméase (transporteur) pour le mélibiose mais elle est inactivée à 42°C ; par contre la souche
peut utiliser LacY (en effet, le transporteur de lactose qui peut aussi transporter le mélibiose) à condition qu’il
soit exprimé. Or le milieu de culture ne contient aucun inducteur donc les seules bactéries qui s’y développent
sont celles qui ont fait « sauter » la répression et expriment donc constitutivement l’opéron lactose.
Préparation du milieu de culture
2 boîtes de Petri renfermant le milieu minimum M63 + mélibiose + X-Gal sont préparés
- réaliser le mélange suivant dans un erlen stérile
. 23,5ml d’agar maintenu en surfusion (à 25g/l)
. 6ml de milieu minimum M63 x5 stérile
. 0,6ml mélibiose stérile 20% (en solution aqueuse)
. 30µl 1M MgSO4-7H2O (stérile)
- bien mélanger (éviter la formation de bulles)
- couler aussitôt en répartissant le mélange dans 2 boîtes de Petri
- laisser sécher prêt de la flamme
- étaler 40 µl X-Gal (2% dans DMF) à l’aide de billes ; bien laisser sécher
Ensemencement
Une culture d’E. coli BL21 en phase exponentielle de croissance vous est fournie.
- mesurer son A600nm après l’avoir diluée au 1/10ème
- étaler 100µl par boîte de la dilution 10-3 (réaliser en milieu minimum M63 de la même manière que
précédemment) à l’aide de billes stériles de la bactérie E. coli BL21. A faire en double.
- placer à 42°C la nuit, boîtes retournées.
Au jour 2
1- Mesure de l’activité β-galactosidase
Vous disposez de 10 prélèvements en final de culture d’E. coli BL21 menées dans 2 conditions différentes (cf.
jour n°1).
Pour la souche étudiée, la culture a été réalisée en présence de lactose ou d’un analogue du lactose non
métabolisé par les bactéries (IPTG).
Les prélèvements effectués (env. 1ml) de chacune des 2 cultures ont été effectués à des temps différents ; le t0
correspond au moment où la culture a atteint la valeur de 0,4 d’absorbance à 600nm juste avant l’addition ou
non de l’inducteur.
Ces prélèvements ont été stockés au froid, ce qui assure la conservation des bactéries.
A partir des culots bactériens, des « extraits » seront préparés dans un premier temps ; cela correspond à la
perméabilisation des cellules. Le traitement que les bactéries subissent désorganise partiellement la membrane
cellulaire, ce qui permet à de petites molécules comme l’ONPG, de diffuser librement dans la bactérie ; le toluène
ou le dichloroéthane associé au SDS sont utilisés pour perméabiliser les cellules.
A partir de ces extraits, un dosage de la β-galactosidase est réalisé dans un deuxième temps.
- à chacun des culots bactériens, ajouter (dans l’ordre) 400µl de tampon Z (+2-ME), 10µl de
SDS 0,1% et 50µl de dichloroéthane (attention lors de la manipulation : à faire sous la
hotte)
- vortexer 10 secondes (minimum) puis placer les tubes eppendorf dans un bain thermostaté
à 37°C pendant environ 5min (pré-chauffage)
- ajouter 200µl d’ONPG (4mg/ml) dans chacun des tubes, mélanger brièvement (par
retournement) et replacer aussitôt les tubes à 37°C ; déclencher votre chronomètre
5
 6
6
 7
7
 8
8
1
/
8
100%